【2020 ASCO 一睹为快】信达生物七项研究入选(下篇), 多瘤种探索免疫治疗疗效与潜能
2020年5月29日至5月31日,一年一度的全球肿瘤领域盛会——美国临床肿瘤学会(ASCO)年会首次在线上召开,以多种形式传递肿瘤学最新进展,分享多学科观点,探讨未来发展。信达生物有7项重要研究发布,本文谨介绍第二部分的内容。
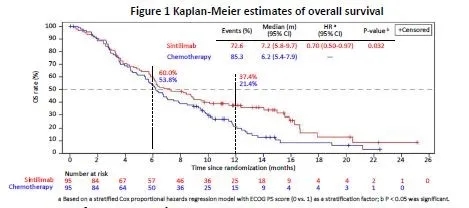
ORIENT-2研究旨在评价PD-1抑制剂信迪利单抗与化疗相比,治疗难治性晚期食管鳞癌患者的疗效和安全性。
研究共纳入190例患者,按1∶1的比例随机分配入信迪利单抗组(200mg,q3w)和化疗组(紫杉醇175mg/m2,Q3W,或伊立替康180mg/m2,q2w),信迪利单抗组的中位总生存(OS)相比紫杉醇/伊立替康化疗组更长,可以显著延长患者总生存期(HR=0.70, P=0.032),信迪利单抗组和化疗组的中位OS分别为7.2个月和6.2个月,12个月OS率分别为37.4%和21.4%,信迪利单抗显示出了令人鼓舞的抗肿瘤疗效。信迪利单抗在食管鳞癌中的安全性特征与其他瘤种相似。
徐建明教授点评
徐建明 教授
解放军总医院第五医学中心消化肿瘤科主任 教授 博士生导师
中国抗癌协会大数据与真实世界专业委员会 副主任委员
中国研究型医院 肿瘤学专业委员会 副主任委员
中国临床肿瘤学会胃肠胰腺神经内分泌肿瘤专业委员会 主任委员
徐建明教授:对于既往接受过一线化疗的晚期难治性食管鳞癌患者,治疗手段极其有限,但是,多项临床研究显示,免疫治疗在晚期食管癌二线治疗中对比化疗取得了令人鼓舞的疗效。信迪利单抗相比化疗可以给一线化疗后的难治性晚期食管鳞癌患者带来生存期的显著延长。
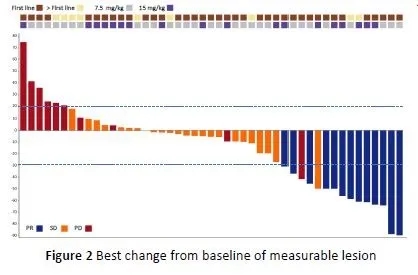
该研究旨在评估信迪利单抗联合不同剂量的IBI305,治疗晚期肝细胞癌的疗效和安全性。研究纳入了50例晚期或转移性肝细胞癌患者,其中41例为一线治疗。分为信迪利单抗200mg联合IBI305 7.5 mg/kg q3w(低剂量组,n=29)以及信迪利单抗200mg联合IBI305 15 mg/kg q3w(高剂量组,n=21)。研究结果显示,低剂量组患者的中位治疗周期为4周期(1~19周期),高剂量组患者的中位治疗周期为11周期(1~16周期)。
安全性方面,治疗相关不良事件大多为1~2级,所有患者最常见的为高血压(28.0%)和发热(26.0%);3~4级不良反应发生率高剂量组为23.8%,低剂量组为仅为3.4%。根据RECIST v1.1标准,低剂量组患者的ORR为24.1%,高剂量组患者的客观缓解率(ORR)为33.3%。数据截止时,中位无进展生存(PFS)尚未达到,6个月的PFS率在低剂量和高剂量组分别为60.5%和 75.8%。
周爱萍 教授
主任医师 内科副主任
中国医学科学院肿瘤医院/国家癌症中心
中国临床肿瘤学会(CSCO)尿路上皮癌专业委员会副主任委员
中国临床肿瘤学会(CSCO)结直肠癌/胃癌/智慧医疗专业委员会常务委员
中国医疗保健国际交流促进会消化道肿瘤MDT分会副主任委员
中国研究型医院学会精准医学与肿瘤MDT专业委员会副主任委员
中国老年学学会老年肿瘤专业委员会 (CGOS)副干事长、胃肠专家委员会副主任委员
周爱萍教授:IBI305为信达生物自主研发的贝伐珠单抗的生物类似药。近来,免疫治疗与抗血管生成治疗药物联合使用已在多个瘤种中显示了良好的疗效,包括肝细胞癌。如在IMbrave150研究中,阿替利珠单抗(抗PD-L1单抗)与贝伐珠单抗联合一线治疗肝细胞癌在ORR、PFS和OS上均显著优于索拉非尼。此研究中信迪利单抗联合低或高剂量的IBI305治疗晚期肝细胞癌,均显示出了富有潜力的疗效。高剂量组在ORR和6个月的PFS率上似乎更具优势,安全性良好。低剂量组则在安全性上更具优势。当然,以上结果还有待进一步扩大样本量和延长随访时间以验证。
【摘要6071】吸入式STING激动剂联合化疗+免疫治疗用于铂耐药或铂难治性卵巢癌:开放、随机对照的Ⅱ期临床研究
由于复发卵巢癌患者的免疫力不佳,免疫检查点抑制剂的治疗有效率仅为10%~15%。在之前的研究中,已经发现激活STING信号通路可以增加免疫治疗敏感性。因此,研究者将STING激动剂MnCL2以及nPP(白蛋白紫杉醇+顺铂)化疗和PD-1抗体信迪利单抗进行联合治疗铂耐药或铂难治性卵巢癌患者。该研究为开放、随机对照的Ⅱ期临床试验,按2∶1随机接受nPP化疗+信迪利单抗加(队列1)或不加(队列2)MnCL2治疗。所有患者既往至少进行过4线治疗,基线中位治疗周期为19周期。截至2020年1月,共入组27例,其中21例纳入疗效分析。在将MnCL2加入化疗和信迪利单抗的联合治疗方案后,未出现治疗相关不良事件的加剧。联合与不联合MnCL2组,最常见的治疗相关不良事件均为血液学毒性(87%)、恶心(56%)和呕吐(47%)。在联合MnCL2组中,队列1的19例患者中,所有14例可评估患者均取得了有效的疾病控制[11例(78.6%)部分缓解(PR),3例(78.6%)疾病稳定(SD)]。在首次疗效评估中,10例(71.4%)患者获PR。队列2的8例中,7例可评估,全部为SD,其中4例的病灶增大,在4周期的治疗后PD。
孟元光教授点评
孟元光 教授
解放军总医院第一医学中心妇产科主任
国家远程医疗与互联网医学中心妇科肿瘤专家委员会主任委员
中国妇幼保健协会妇科智能医学专业委员会主任委员
中华医学会妇产科分会委员
中华医学会妇科肿瘤学分会委员
中国医师协会妇产科分会常委
中国医师协会医学机器人分会常委
全军第十届医学科委会妇产科专业委员会副主任委员
2014年科学中国人年度人物
2018年第二届国家名医盛典当选为“国之名医”
担任多家杂志的常务编委和编委
孟元光教授:卵巢癌是妇科三个恶性肿瘤之一,尽管发病率比宫颈癌和内膜癌要低,但是卵巢癌的预后一直是困扰国际国内妇科肿瘤专家的一个问题。尤其对于铂耐药、难治复发型的这类患者,尽管现在一些靶向药物出现比如PARP抑制剂以及免疫检查点抑制剂PD1、PD-L1的出现,使得我们看到了一线希望。然而免疫治疗在卵巢癌领域一些临床试验的效果并不是完全好,但其中也发现了免疫治疗的拖尾效应,特别在有效患者中持续效应好。这使我们看到免疫治疗在卵巢癌领域的希望,如何使免疫治疗做进一步的改善?实际上免疫治疗大家做了很多复合型的临床研究,比如说免疫+免疫、免疫+化疗、免疫+放疗、免疫+抗血管生成药物, 包括近期我们所做的STING激动剂联合化疗+PD-1的临床试验。虽然很多复合型临床试验的结果还没有公布,但是从我们中期分析来看,结果令我们欢欣鼓舞。但是这毕竟是Ⅱ期的试验结果,随访时间还未达到我们所期望的终点,同时安全性,客观缓解率还要继续期待。我们会在此基础上完善我们的试验,包括进一步扩大样本量。希望通过这种治疗,能给卵巢癌尤其是铂耐药和复发难治型的这些患者带来福音,同时为这两种类型的治疗开创新的临床思路。
韩为东 医学博士 教授 研究生导师
解解放军总医院第一医学中心生物治疗科主任
首都科技创新领军人才
原总后勤部科技新星
中国研究型医院生物治疗学专业委员会首届主任委员
先后承担科技部重大专项1项、973课题2项、863项目3项、国家自然基金重大项目1项、重点项目2项、国家发明专利20余项
主编专著3部
以第一作者或通讯作者发表SCI论文160余篇
韩为东教授:铂类抵抗的复发难治性卵巢癌患者治疗手段有限,无论是化疗还是抗血管靶向药,以及单用PD-1抑制剂,或者化疗联合PD-1抗体药物等不同组合,整体临床响应率比较低,本研究是一个随机的2∶1对照的、单盲的临床研究,试验组加入了STING激动剂,其中还包括有几例患者是使用PARP1抑制剂失败后入组的,初步的中期总结报告显示,加入STING激动剂后的患者客观缓解率有明显提高,之后,我们还需要继续扩大临床入组量来验证这一点,但主要还要看患者的PFS与生活质量的改善情况,对这个研究我们还是非常有信心,该组合疗法的短期,长期效果也值得期待。
该研究旨在评估IBI310单药或与PD-1抑制剂信迪利单抗联合治疗晚期黑色素瘤的疗效和安全性。研究分为A、B、C 3个部分,A部分的晚期黑色素瘤患者接受IBI310治疗,以加速滴定(0.3 mg/kg IBI310(q3w,IV))结合3+3爬坡设计(1、2 或 3 mg/kg IBI310(q3w,IV)),最多治疗3周期;B部分以3+3爬坡给予1、2 或 3 mg/kg IBI310(q3w,IV)联合信迪利单抗(200 mg,q3w,IV),共4周期,然后以信迪利单抗维持治疗(200 mg,q3w,IV);C部分是联合疗法的扩展研究。A部分入组10例患者,B和C部分共入组17例。研究结果显示,A、B两部分无DLT发生,A部分中,9例患者出现治疗相关不良事件,常见的为瘙痒(4例)、促甲状腺激素升高(2例)以及乏力(2例),无3级及以上不良反应事件发生。5例患者SD。在B、C两部分中,13例患者出现治疗相关不良事件,仅1例发生3级治疗相关不良事件(3mg剂量,出现天冬氨酸转氨酶升高),其他为2级,最常见的为瘙痒(8例)、皮疹(7例)和丙氨酸转氨酶升高(6例),无致死性不良事件发生。在信迪利单抗联合治疗的可评估患者中,IBI310 2mg/kg组中7例有1例获得确认的PR,IBI310 3mg/kg组3例有1例获得确认的PR,5例SD。C部分的研究尚在进行中。
郭军教授点评
郭军 主任医师 博士生导师 教授
北京大学肿瘤医院副院长
北京市肿瘤防治研究所副所长
中国临床肿瘤学会(CSCO)副理事长
CSCO黑色素瘤专家委员会主任委员
CSCO肾癌专家委员会副主任委员
CSCO免疫治疗专委会副主任委员
CSCO尿路上皮癌专委会副主任委员
亚洲黑色素瘤协作组主席
CFDA药品注册评审专家(肿瘤组)
国家卫生计生委合理用药专家委员会委员(抗肿瘤用药专业组)
郭军教授:IBI310是针对CTLA-4的人源化IgG1单克隆抗体。IBI310单克隆抗体单药或与信迪利单抗联合治疗晚期黑色素瘤耐受性尚好,副反应与既往报道无明显差异。在临床研究中,我们发现这种联合治疗对于大瘤负荷的肢端型黑色素瘤出现了明显的肿瘤退缩。因为肢端型黑色素瘤不同于皮肤黑色素瘤,对PD-1单抗单药不敏感,大瘤负荷就更难看到疗效了,这些案例研究初步证明了双免联合治疗在晚期黑色素瘤,特别是在肢端黑色素瘤中的抗肿瘤活性。这种联合模式已被引入到肢端黑色素瘤术后辅助治疗的临床研究中,该研究已在我中心于今年4月率先启动,是国际上首个大型的随机、全国多中心Ⅲ期,针对肢端型黑色素瘤的辅助治疗研究,希望这种联合能为中国的肢端型黑色素瘤患者带来突破。