“现货”NK细胞疗法进行首个急性髓细胞性白血病患者给药,Carl June博士看好NK细胞在肿瘤免疫领域的发展
近日,临床阶段生物制药公司Kiadis Pharma宣布,首位复发/难治性急性髓细胞性白血病(r/r AML)患者在俄亥俄州立大学综合癌症中心——詹姆斯癌症医院(OSUCCC-James)成功进行K-NK细胞给药。
该K-NK细胞是基于Kiadis公司专有的FC21和通用供体平台,在OSUCCC-James细胞治疗实验室生产的“现货”NK细胞疗法。预计将为Kiadis公司的NK细胞候选产品K-NK003的开发计划提供宝贵的数据。
试验设计
该 I 期临床研究(NCT04220684)将在56位原发性难治性AML和骨髓增生异常综合征( MDS)患者中评估K-NK细胞,受试者将在接受减毒化疗后,接受六剂剂量为 1x107 细胞/ kg至 1x108 细胞/ kg的NK细胞。
该研究的主要目标是评估K-NK细胞的安全性,次要目标是评估缓解率以及最佳剂量。该实验结果有望为Kiadis的K-NK003产品提供进一步的临床概念验证。
OSUCCC-James的细胞治疗实验室的医学总监、该临床实验的主要研究者Sumithira Vasu表示:“这种通用供体来源的NK细胞疗法对于r/r AML和MDS患者来说,是一种令人兴奋的新的实验治疗选择,能够在需要的时立即注入大量功能性的NK细胞。目前这种疗法已经完成了第一名患者给药,是我们临床研究中的重要一步。”
Kiadis的首席医学官Andrew Sandler评论说:“该实验使用了一种新型的、“现成”的NK细胞产品来治疗一组病重且难以治疗的患者。我们对这项实验非常激动,并且这为使得我们将K-NK细胞疗法推向更广泛的癌种群众又迈出了一步。”
Kiadis Pharma
Kiadis Pharma成立于1997年,正在努力成为一家完全集成的生物制药公司,致力于为威胁生命的疾病开发创新疗法。Kiadis于2015年7月2日在泛欧证券交易所阿姆斯特丹交易所、布鲁塞尔交易所上市,股票代码为KDS。2019年4月,Kiadis公司成功收购了CytoSen Therapeutics。
Kiadis的总部位于荷兰阿姆斯特丹,并在美国各地设有办事处,该公司旨在利用人类的自然力量和集体免疫系统提供最佳细胞,从而重新构建医学。目前,该公司的重点研发项目是NK细胞疗法。
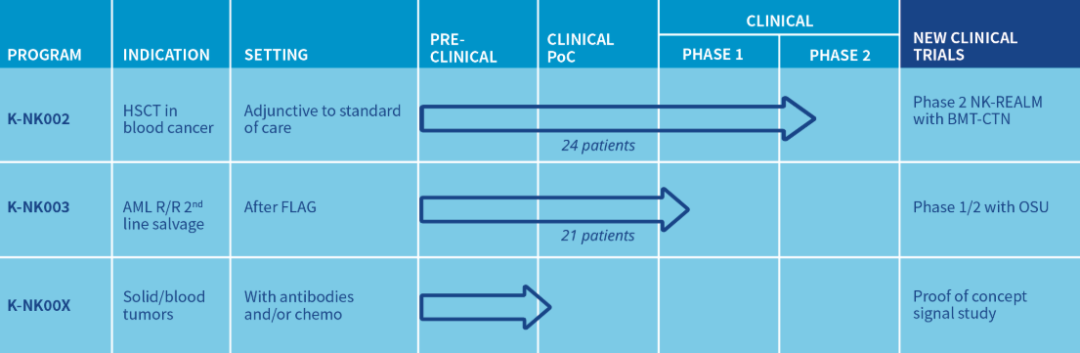
基于该公司专有的独特的通用供体平台来源的NK细胞,和PM21粒子离体增殖和激活技术,Kiadis开发了涵盖血液瘤和实体瘤的多款“现货”或/和单倍体NK细胞项目,以便更快速、更经济的提供给广泛的受众。
-
K-NK002:是Kiadis进展最快的NK细胞候选产品,目前正在进行 II 期临床试验,以评估单倍同型供体的NK细胞在防止AML和MDS移植后复发的作用。该研究是基于MD安德森癌症中心积极的临床前数据而设计的:完全缓解率(CR)为69%,历史CR为20%-26%。
-
K-NK003:正在进行 I/II 期临床试验,以评估NK细胞作为r/r AML的治疗方法。
-
K-NK00X:目前正在作为治疗方法进行血液瘤和实体瘤的临床前研究。
NK细胞疗法
众所周知,NK细胞在人体的先天免疫系统中起着重要的作用,早在上个世纪70年代,科研人员就对它们进行了描述,但直到最近的15年,人们才逐渐了解NK细胞在帮助抗击癌症和其它疾病方面的复杂性和治疗潜力。
目前,NK细胞疗法已经成为一个炙手可热的领域。自然杀伤细胞(natural killer cell, NK细胞)是人体先天免疫系统的一部分,能对身体内遇到的各种病原体迅速作出反应,是抵御危险感染或异常细胞的第一道防线,是身体对抗癌症的正常储备。
与其他免疫细胞(T细胞、B细胞)不同的是:通常情况下,T细胞需要检测到靶细胞表面的MHC,才会引起细胞因子的释放,进而导致靶细胞裂解或凋亡;而NK细胞可以在没有抗体或MHC的情况下,识别这些细胞并进行快速的免疫响应。
因NK细胞不同于T细胞的非特异性识靶及杀伤机制,吸引了众多的研究者和投资者的关注。
2018年10月1日,Dragonfly Therapeutics宣布与默沙东公司达成了一项高达6.95亿美元的许可协议,默沙东将可以获得使用TriNKET™平台开发的一系列实体瘤项目的专有权。双方既没有公开项目的数量,也没有公开实体瘤的类型。
2018年12月13日,Celgene公司更是以总计2400万美元的预付款、未来的里程碑和特许权使用费,获得Dragonfly Therapeutics的2种TriNKET™免疫治疗候选药物的授权许可。
2019年9月,Nkarta Therapeutics获得了由Samsara BioCapital领投的1.14亿美元B轮融资,以支持其“现货”NK细胞产品的临床开发计划。Nkarta的主要候选产品NKX101,是一款靶向NKG2D的同种异体NK细胞,目前正在血液瘤和实体瘤中进行临床试验。
2020年4月2日,Fate Therapeutics宣布,与强生(Johnson & Johnson)旗下杨森(Janssen)生物科技公司达成了高达31亿美元的合作协议,该合作将利用Fate公司的iPSC产品平台和杨森公司专有的肿瘤抗原binders来创建新型CAR-NK和CAR-T细胞候选产品。
此外,还有其它不少大型制药公司都纷纷布局NK细胞领域,例如武田(Takeda)、艾伯维(AbbVie)、BMS/Celgene等。