RAS(包括KRAS,NRAS和HRAS)是癌症中突变频率最高的基因家族,存在于约24%的癌症,并且是许多癌症的驱动基因。然而,尽管经过30多年的努力,靶向KRAS的抑制剂绝大多数以失败告终,而RAS也被冠以“不可成药”的称号。
2013年底报道的KRASG12C抑制剂ARS-1620及随后其在动物模型中获得的成功让RAS特异性小分子抑制剂的研发初现曙光。2020年9月20日,首个KRASG12C抑制剂Sotorasib临床试验结果在ESMO正式公布,论文也同期发表于《新英格兰医学杂志》(NEJM)。
NEJM医学前沿邀请了北京协和医院胸外科梁乃新教授撰写述评,解读这项堪称里程碑的临床研究。
KRAS p.G12C突变发生于13%的非小细胞肺癌(NSCLC)以及1%~3%的结直肠癌和其他癌症。突变的KRAS蛋白一直被视为“不可成药”,原因是其对GTP的亲和力高且缺乏可利用的结合口袋。目前尚无任何靶向癌症KRAS突变的疗法通过审批。Sotorasib是选择性、不可逆性靶向KRAS p.G12C的小分子,优化了与之前未被利用的一个表面凹槽之间的不可逆相互作用,使得效力和选择性得到增强,从而有可能解决携带KRAS p.G12C突变的肿瘤患者治疗难题。
在一项由M.D. Anderson癌症中心David S. Hong教授和纪念斯隆-凯特琳癌症中心Bob T. Li教授领导的Sotorasib 1期研究中,共计129例携带KRAS p.G12C突变的晚期实体瘤患者(59例NSCLC患者、42例结直肠癌患者和28例其他肿瘤患者)被纳入了剂量递增和扩展队列。剂量递增队列(1至4)计划的剂量水平为180、360、720和960 mg。有107例患者(82.9%)停止治疗;最常见的停止治疗原因是疾病进展。中位治疗持续时间为3.9个月(范围,0~16.6)。共计74例患者(57.4%)接受了≥3个月治疗,38例患者(29.5%)接受了≥6个月治疗。
本研究未观察到剂量限制性毒性作用或与治疗相关的死亡。共计73例患者(56.6%)发生了与治疗相关的不良事件;2例患者(1.6%)发生了严重不良事件。共计15例患者(11.6%)报告了与治疗相关的3级或4级不良事件。与治疗相关的3级不良事件包括丙氨酸转氨酶(ALT)水平升高(4.7%的患者)、腹泻(3.9%)、贫血(3.1%)、天冬氨酸转氨酶(AST)水平升高(2.3%)、血液碱性磷酸酶水平升高(1.6%)、肝炎(0.8%)、淋巴细胞计数减少(0.8%)、γ-谷氨酰转移酶水平升高(0.8%)和低钠血症(0.8%)。1例患者(0.8%)报告了与治疗相关的4级ALT升高,ALT水平在Sotorasib降低剂量,糖皮质激素逐渐降低剂量后恢复至基线水平;1例患者(0.8%)因与治疗相关的3级ALT和AST水平升高而停药。
共有78例患者(60.5%)接受过≥3线治疗,75%的NSCLC患者和98%的结直肠癌患者接受过≥2线治疗。在59例NSCLC患者中,53例(89.8%)接受过PD-1或者PD-L1抑制剂治疗,所有患者(100%)均接受过铂类化疗。由于本试验纳入的大多数患者既往接受过大量、各种模式的药物治疗,转移性疾病接受过的抗癌治疗的线数中位数为3(范围,0~11),因此上述安全性数据非常难能可贵。
129名患者安全性数据
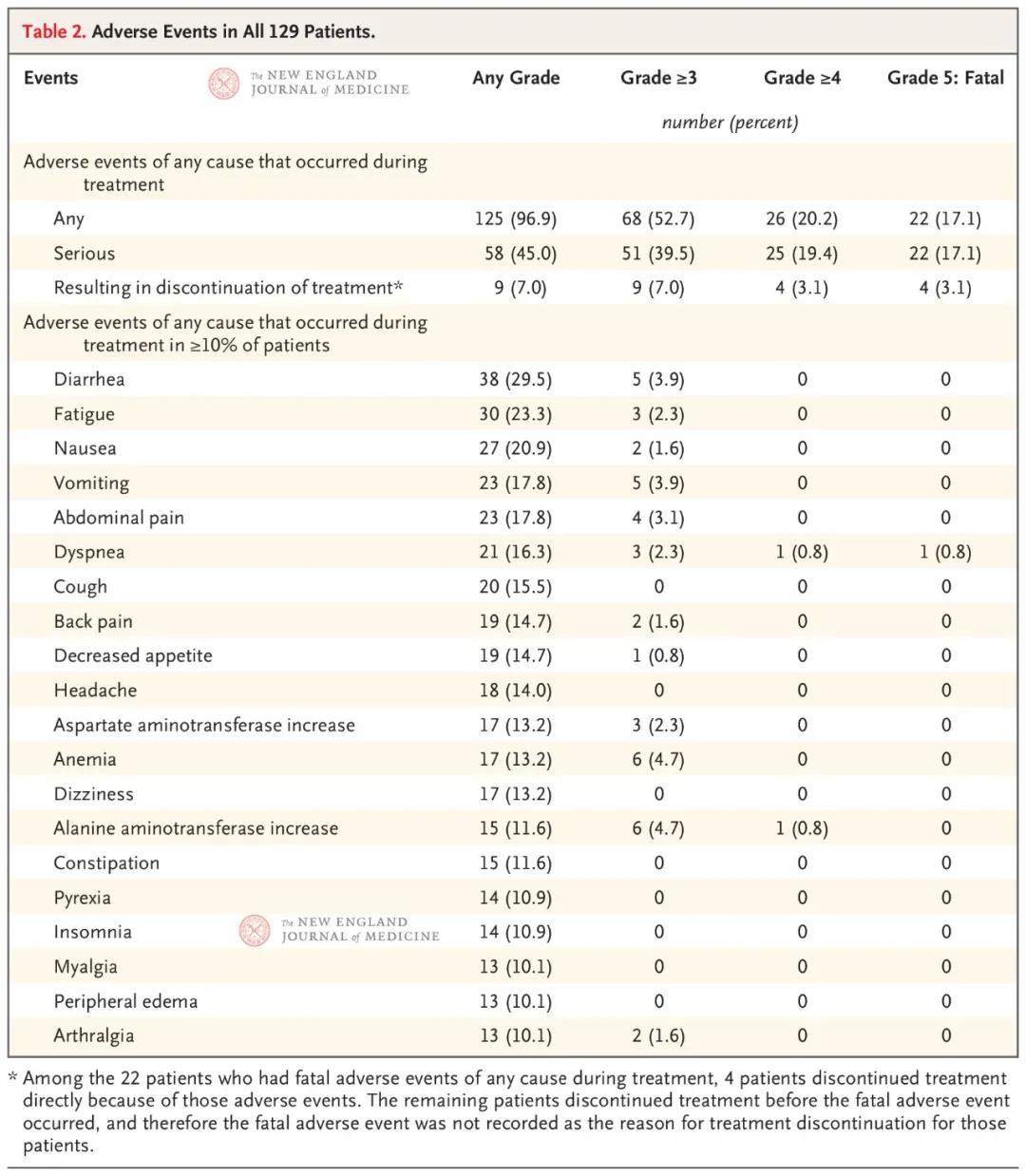
59例NSCLC患者亚组中位随访时间为11.7个月(4.8~21.2),中位无进展生存期为6.3个月。19例达到了经证实的部分缓解,33例达到了疾病稳定;因此,32.2%的患者(20.62~45.64)达到了经证实的缓解,88.1%(77.07~95.09)达到了疾病控制。在960 mg队列的34例患者中,35.3%(12例患者)达到了经证实的缓解,91.2%(31例患者)达到了疾病控制。
42例结直肠癌亚组的中位随访时间为12.8个月(9.0~20.9)。7.1%(3例患者)达到了经证实的缓解,73.8%(31例患者)达到了疾病控制;中位无进展生存期为4.0个月(0.0+~11.1+)。接受每日960 mg剂量治疗的队列包含25例患者,其中12.0%(3例患者)达到了经证实的客观缓解,80.0%(20例患者)达到了疾病控制。
在其他类型肿瘤患者中,4例达到了经证实的部分缓解(1例胰腺癌、1例子宫内膜癌、1例阑尾癌和1例黑色素瘤),17例达到了疾病稳定,4例发生了疾病进展。4例患者的缓解分别持续4.4、6.9+、2.7和5.6个月。
Sotorasib在所有被试肿瘤中的优效性
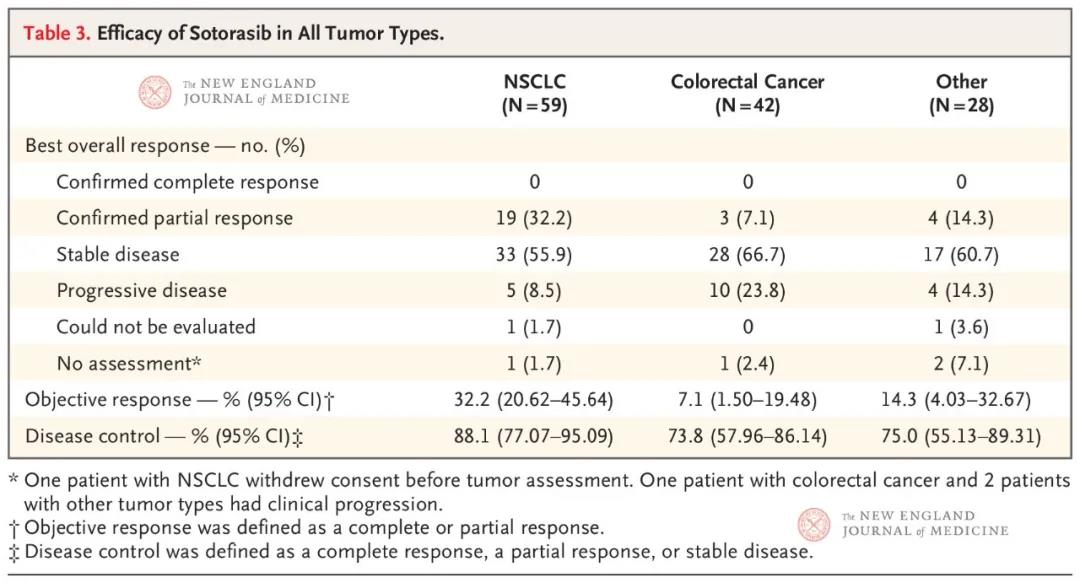
这是第一项揭示Sotorasib在接受过大量治疗且携带KRAS p.G12C突变的实体瘤患者中表现出良好抗癌前景的研究,具有里程碑性意义。限于I期研究及患者数量,我们暂时还不能全面揭示Sotorasib的临床功效。但就目前数据的分析,会给我们带来一些重要思考和提示。
在多线治疗后的晚期实体瘤患者中,仅有73例患者(56.6%)发生了与治疗相关的不良事件,且毒性作用以低级别胃肠道和肝脏毒性为主。即使长期用药也未观察到Sotorasib有剂量限制性毒性作用。
在NSCLC亚组中,所有剂量水平32.2%的缓解率和目标剂量(960 mg)下35.3%的缓解率尤其表现出潜力,提示较好的安全性情况下剂量-疗效的正相关性。
在NSCLC亚组中,所有剂量水平32.2%的缓解率和目标剂量(960 mg)下35.3%的缓解率尤其表现出潜力。在第6周进行的第一次评估中就能观察到Sotorasib治疗后患者的迅速缓解。
有32.2%的NSCLC患者达到了经证实的缓解,且大多数患者(88.1%)达到了持续数月或更长时间的疾病控制,并因此使得中位无进展生存期达到6.3个月。结直肠癌亚组的大多数患者达到了疾病控制,疾病稳定的中位持续时间为5.4个月,中位无进展生存期为4.0个月。采用现行疗法的情况下,仅有9%~18%的NSCLC患者可在接受二线或三线治疗后达到缓解,中位无进展生存期为2.5~4.0个月;在既往接受过治疗的结直肠癌患者中,约有1.0%~1.6%会在接受标准治疗后达到缓解,中位无进展生存期仅为1.9~2.1个月。因此,与本试验中患者相似的NSCLC或结直肠癌患者的治疗结局通常较差,而本试验中这些患者接受Sotorasib治疗后达到的疾病缓解和疾病稳定令人鼓舞。
NSCLC和结直肠癌患者接受治疗后的应答情况不一致,这提示KRAS p.G12C可能并非结直肠癌的主要致癌驱动基因,也可能有其他通路(例如Wnt或EGFR通路)在KRAS之外介导了致癌信号传导。
Sotorasib在接受过大量治疗且携带KRAS p.G12C突变的实体瘤患者中表现出良好的安全性和有效性。在NSCLC或其他实体瘤患者中,进一步评估Sotorasib单药治疗或者Sotorasib与各种药物联合治疗的试验正在进行中(在ClinicalTrials.gov注册号为NCT04303780和NCT04185883)。我们还应注意到,目前的Sotorasib单药疗效还有很大提升空间,在可靠数据和理论指导下的联合疗法未来或可使患者达到完全缓解。
梁乃新,博士,北京协和医院胸外科副主任医师,硕士生导师。现任中华医学会胸心血管外科分会青年委员,中国医师协会胸外科分会青年委员,北京医学会胸外科分会青委会副主任委员,北京健康促进会副会长等学术兼职。国家医学考试中心执业医师考试特聘专家。长期专注于肺癌以手术为基础的精准医学全程管理。获得国家及省部级基金5项,各类课题10余项,作为第一或通讯作者在国际知名杂志发表论著三十余篇。


