2022年4月13日,全球首个不区分肿瘤来源的广谱靶向药--larotrectinib(硫酸拉罗替尼胶囊,Vitrakvi ®,下文统称拉罗替尼)终于获得中国国家药品监督管理局批准正式上市,用于治疗患有NTRK基因融合的局部晚期或转移性实体瘤的成人和儿童患者!同时也有了响当当的大名-维泰凯®。
拉罗替尼于2018年11月26日获FDA批准上市,用于治疗患有NTRK基因融合的局部晚期或转移性实体瘤的成人和儿童患者,是一种广谱抗癌靶向药,在多种肿瘤中有效性一致,包括肺癌,黑色素瘤,结直肠癌,胃肠道间质瘤,乳腺癌,骨肉瘤,胆管癌,软组织肉瘤,唾液腺瘤,婴儿纤维肉瘤,甲状腺癌,原发性未知癌,先天性中胚层肾癌,阑尾癌和胰腺癌。
拉罗替尼为NTRK基因抑制剂,NTRK基因家族包括NTRK1、NTRK2和NTRK3,这些基因如果与其它基因发生融合,可导致异常激活,从而引起肿瘤的发生。NTRK基因融合在多种肿瘤中都有发现,拉罗替尼则是治疗该类肿瘤的第一选择。
2022年6月23日,国家药品监督管理局(NMPA)正式批准了硫酸拉罗替尼口服溶液(larotrectinib)的上市申请。Larotrectinib是一款“不限癌种”疗法,它是全球首款专为NTRK基因融合癌症患者设计的口服TRK抑制剂。在中国,这款新药的胶囊剂型于今年4月首次获批上市。
拉罗替尼 维泰凯 Larotrectinib(Vitrakvi) (LOXO-101,ARRY-470)美国上市时间:2018年11月26日 批准单位:美国食品和药物管理局(FDA) 药物名称:Vitrakvi(又名Larotrectinib) 药物功效:有效对抗由单一罕见TRK融合基因突变驱动的各种癌症 针对群体:局部晚期或转移性实体瘤的成人和儿童患者 制造商:Bayer(拜耳)和Loxo Oncology共同研发 靶点:针对有NTRK1、NTRK2或者NTRK3基因融合的肿瘤患者
※推荐剂量 (1)如果患者的体表面积≥1m 2 ,每天二次,每次100mg ,空腹或随餐口服。 (2)如果患者的体表面积<1m 2 ,每天二次,每次100mg/m 2 ,空腹或随餐口服。如果漏服,发现时若离下次服药6 小时以上,可以按量补服,下次服药仍按照原间隔时间。如果服药后发生呕吐,不可补服,下次服药仍按照原间隔时间。 ※剂量调整 如果发生3/4级不良反应,暂停Larotretinib ,按表1减量直至症状缓解至1级以下,在四周内缓解可按表1减量重新服用。如果症状在四周后仍无法缓解,永久停用Larotretinib 。
应避免与强效CYP3A4抑制剂同时使用,如果不可避免时,将Larotretinib的剂量减半,停用CYP3A4抑制剂3-5个半衰期后,恢复Larotretinib原剂量。 应避免与强效CYP3A4诱导剂同时使用,如果不可避免时,将Larotretinib的剂量加倍,停用CYP3A4诱导剂3-5个半衰期后,恢复Larotretinib原剂量。 对于中至重度肝损害(Child-Pugh B级和C级)患者,Larotretinib的剂量减半。
胶囊:25mg和 100mg。 口服溶液: 20 mg/mL。
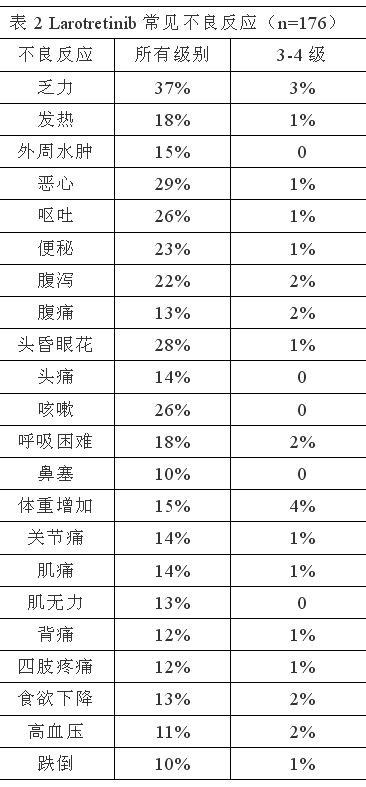
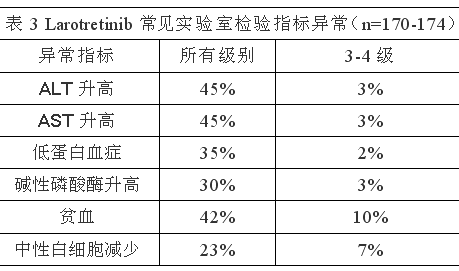
※神经毒性 176例服用Larotretinib的患者,神经毒性发生比例为:所有级别53%,3级6%(包括谵妄2%,构音障碍1%,头昏眼花1%,行走障碍1%和感觉异常1%),4级脑病1例(0.6%)。65%的患者在服用Larotretinib的第一个月发生神经毒性。7%的患者因神经毒性而减量。当患者发生神经毒性时,不可驾驶或操作危险机器。 ※肝毒性 176例服用Larotretinib的患者,肝毒性发生比例为:所有级别45%,3级ALT或AST升高比例6%,4级ALT升高1例(0.6%)。中位肝毒性发生时间为2个月。4%的患者因AST升高减量,6%的患者因ALT升高减量,2%的患者因ALT或AST升高永久停药。服药第一个月,每二周检查肝功能,之后每月复查一次或按医嘱。 ※胚胎-胎儿毒性 动物试验显示,Larotretinib有胚胎-胎儿毒性。患者和伴侣应在服药期间和停药一周内,使用有效的避孕措施。 ※常见不良反应 最常见不良反应(≥20%):疲劳, 恶心, 头晕, 呕吐, 贫血, AST升高, 咳嗽, ALT升高, 便秘和腹泻。常见严重不良反应(≥2%):发热,腹泻,败血症,腹痛,脱水,蜂窝织炎和呕吐。54%的患者发生3级和4级不良反应,37%的患者因不良反应暂停或减量,13%的患者永久停药。 常见停药原因(比例分别为1-2%):脑水肿,肠穿孔,心包积液,胸腔积液,小肠梗阻,脱水,疲劳,ALT升高,AST升高,肠外瘘,淀粉酶升高,脂肪酶升高,肌无力,腹痛,哮喘,食欲下降,呼吸困难,低钠血症,黄疸,晕厥,呕吐,急性髓系白血病和恶心。最常见暂停或减量原因(≥3%):ALT升高(6%),AST升高(6%)和头昏眼花(3%)。导致减量的不良反应82%发生在服药头三个月。 常见不良反应(≥10%)和实验室检验指标异常((≥5%)见表2和表3。
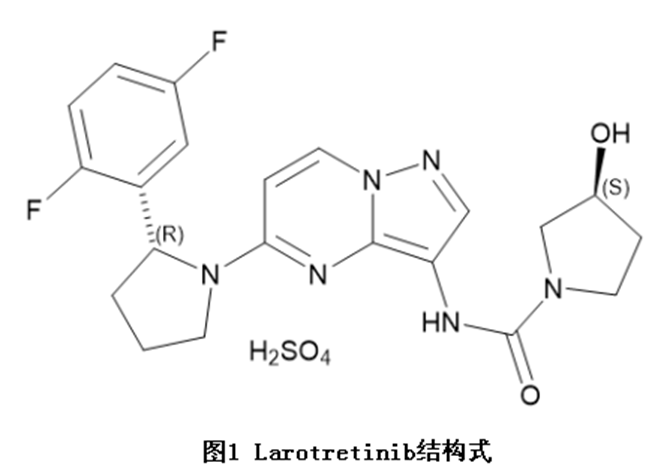
Larotretinib胶囊和口服溶液是硫酸盐,结构式见图1 ,分子量526.51 克每摩尔。Larotretinib硫酸盐是灰白色至粉黄色固体,不吸湿,3 7℃下,pH1.0时极易溶于水,pH6.8时易溶于水。100mg Larotretinib胶囊相当于123mg Larotretinib硫酸盐。
Larotretinib是一种原肌球蛋白受体激酶(TRK)A/B/C抑制剂,对NTRK 1/2/3基因融合敏感,对TRKA和TRKC激酶结构域突变耐药,比如G595R,G623R,G696A和F617L等突变。 Larotretinib服药1 小时后达到血药浓度峰值,平均半衰期为2.9 小时,3 天后达到稳态,C max 平均值为788ng/mL 。血浆蛋白结合率70% ,表观清除率98 升每小时。Larotretinib胶囊的平均生物利用度为34%,口服溶液的AUC类似,C max 升高36%。健康人与高脂食物同服Larotretinib胶囊时,和空腹口服比较,AUC类似,C max 减少35%。 Larotretinib主要通过肝CYP3A4 酶代谢,它是BCRP 和P-gp 的底物。年龄,性别和体重对Larotretinib的代谢没有临床意义上的影响。终末期肾病(需要透析)患者服用Larotretinib时,AU C升高1.5倍,C max 升高1.3倍。对于轻度肝损害(Child-Pugh A级)患者,AU C升高1.3倍,C max 类似;对于中度肝损害(Child-Pugh B级)患者,AU C升高2倍,C max 类似;对于重度肝损害(Child-Pugh C级)患者,AU C升高3.2倍,C max 升高1.5倍。 如果与强效CYP3A4抑制剂合用,将会显著增加血药浓度,比如联用伊曲康唑时,Larotretinib的Cmax升高2.8倍,AUC升高4.3倍.。 如果与强效CYP3A4诱导剂合用,将会显著降低血药浓度,比如联用利福平时,Larotretinib的Cmax↓71%,AUC↓81%。 如果与强效P-gp 抑制剂合用,将会显著增加血药浓度。原英文说明书中,此处为利福平,显然有误,利福平是P-gp 诱导剂。 如果与强效CYP3A4底物合用,将会显著增加血药浓度,比如联用咪达唑仑时,Larotretinib的Cmax和AUC升高1.7倍.。
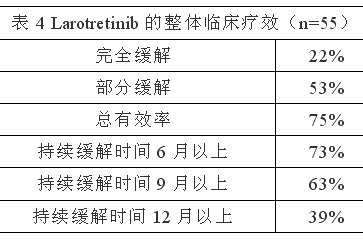
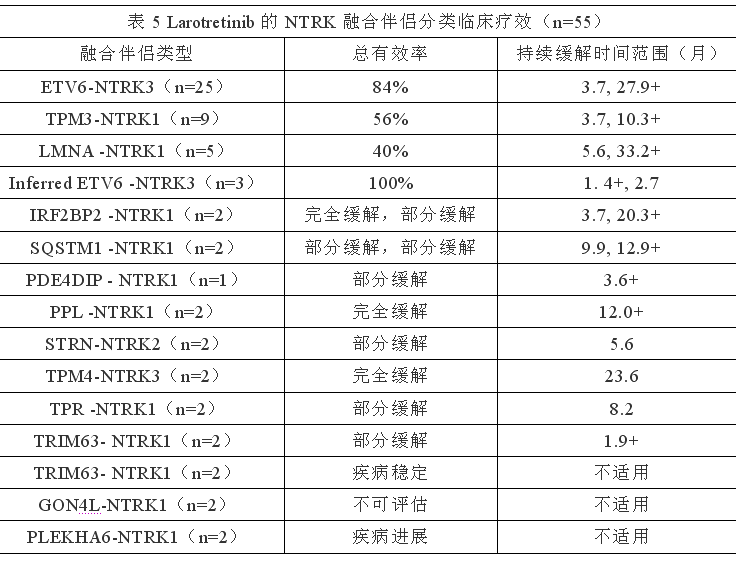
LOXO-TRK-14001, SCOUT和NAVIGATE三个临床研究里的55例NTRK融合实体瘤患者可供评估疗效,中位年龄45岁,22%小于18岁,53%男性,67%白人,93%PS评分为0-1,82%晚期,18%局部晚期并不可手术,98%之前接受过手术或放疗或全身治疗,82%之前接受过2种(中位值)全身治疗,35%之前接受过3种以上全身治疗。50例患者NTRK融合NGS阳性,5例患者NTRK融合FISH阳性。 临床疗效见表4,表5和表6。
胶囊于室温(20 ℃-2 5℃)保存,避免受潮,允许短期储存于15 ℃-30 ℃环境下。 口服溶液储存于冰箱, 2 ℃-8 ℃,不可冷冻。
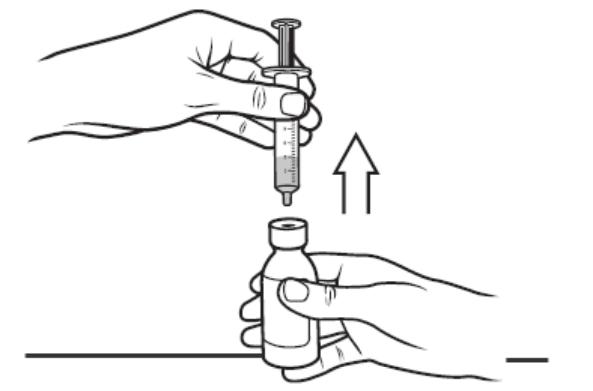
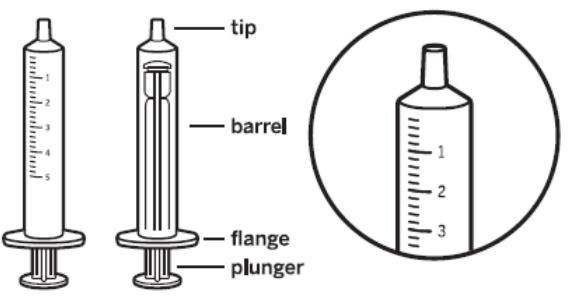
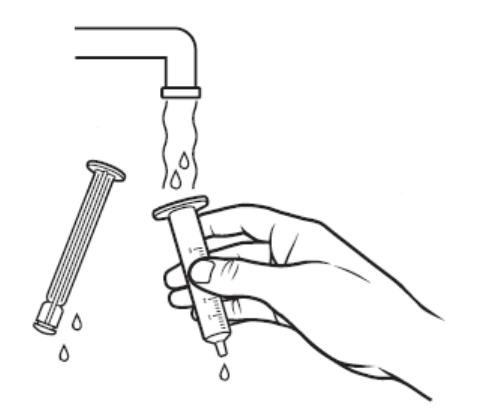
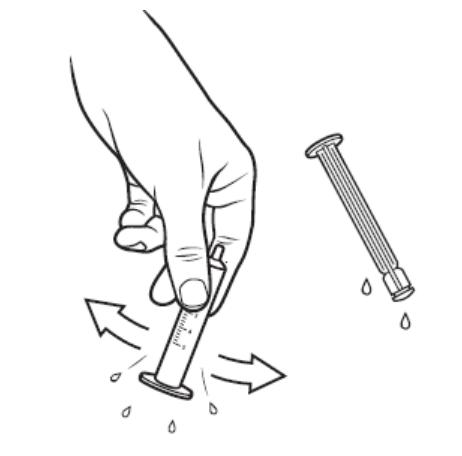
Larotretinib口服溶液为玻璃瓶包装,配有瓶口接头一个,1mL或5mL口服注射器一支(用纯净水清洗后晾干可重复使用一周),见下图。
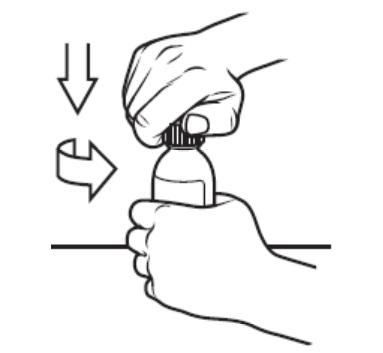
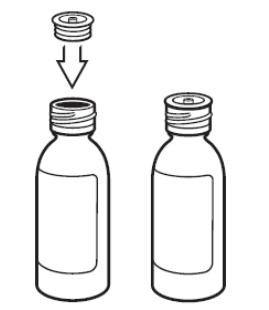
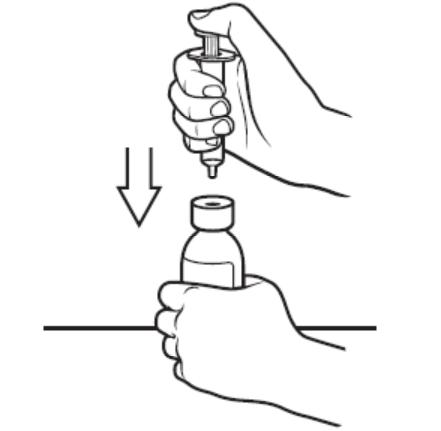
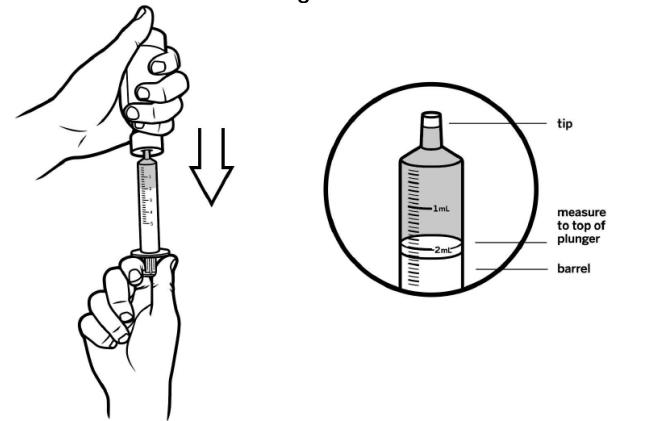
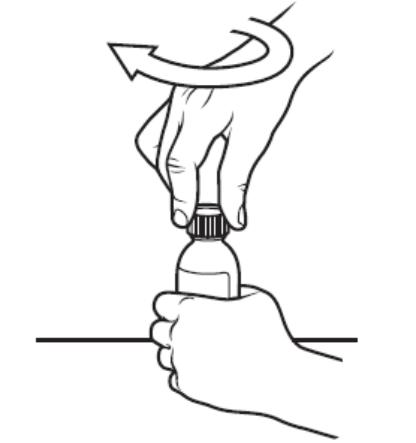
用力按下瓶盖,逆时针旋转瓶盖,取下瓶盖后,塞入接头。注射器排净空气后插入药瓶,倒置药瓶,抽取所需体积的溶液,注意排净气泡
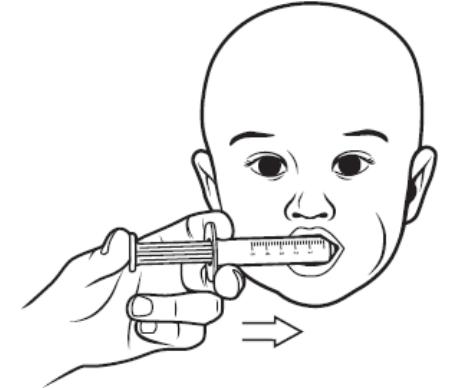
。再把药瓶回正,取出注射器。取下接头,盖回瓶盖。把注射器头部塞入患儿口内,缓慢挤入溶液。服药期间和服药后几分钟,患儿保持挺身姿势。
|
|---|