科学家们到底能否开发出潜在有效的HIV疫苗?

2016年12月19日 讯 /生物谷BIOON/ --一旦接种,终生免疫,这是成千上万名从事HIV研究的科学家们的研究目标,HIV能够阻止机体的免疫系统以及疫苗发挥作用,然而HIV在躲避机体免疫系统的成功或许就能够帮助研究者进行疫苗研究来开发出治疗多种疾病的疗法,比如流感、丙肝、蚊传播的疟疾、登革热和西尼罗病毒感染等。
那么HIV到底是以什么方式来保护自身免于免疫系统的攻击呢?而这种方式又是如何帮助研究者开发抵御其它感染性病原体的新型疫苗呢?
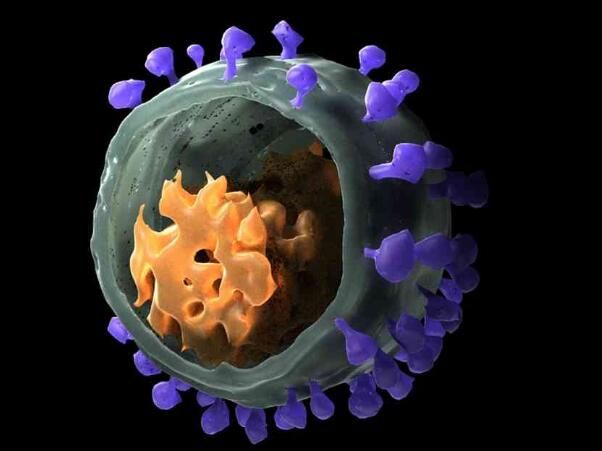
HIV可以躲开免疫系统
HIV有着一系列诡计能够躲避机体免疫系统的攻击作用,在机体应对感染的免疫反应期间,抗体能够锁定病毒表面的靶点来使得这种传染性的威胁失活;为了避免遇到这种情况,HIV就会改变自身的形状以便隐藏能被抗体识别并靶向作用的靶点,这样一来抗体即便对病毒表面进行扫面,也并不会锁定病毒靶点。
同样,HIV还能够适应并且模拟机体的其它蛋白,这对于免疫系统鉴别并且攻击外来病原体至关重要,但这并不会靶向作用且损伤机体的正常细胞,因此当HIV改变自身结构来模仿机体其它正常部分时,免疫系统就会上当受骗。
由于HIV会采用多种方法来躲避免疫系统的靶向杀灭作用,因此如今HIV依然是影响全球人群健康的重大公共卫生负担,仅2015年就有180万儿童感染HIV,而且有110万人死于和HIV相关的疾病。
能够打败HIV的新一代疫苗
“精英控制者”(elite controllers)是一些感染了HIV的人在不用药物的情况下还能保证机体不发病的人群,患者机体的免疫系统通常能够有效地控制病毒的发展;当研究者深入剖析机体免疫系统时,他们在这些精英控制者机体中发现了非常罕见的抗体,这些抗体能够结合许多不同“版本”的病毒,相比正常抗体而言,这些抗体机具粘性和潜力,起能够“紧紧抓住”病毒的其它部位对病毒实施控制,因此这些病人机体的免疫系统能够更好地抑制病毒快速复制以及对机体的损伤作用。
目前研究者关注的焦点就是开发新一代抵御HIV的疫苗,即教会免疫系统如何制造和“精英控制者”机体中相似的罕见抗体;标准的疫苗注射包括向个体机体注射无活性的全毒株或部分病原体来刺激机体产生免疫力;对于HIV而言,研究者首先需要鉴别出特殊的抗体,能够抑制病毒发生改变;随后研究者将会设计出一种疫苗策略来促进机体免疫反应产生特殊的抗体,这就包括利用不同版本的疫苗来进行多次注射从而指导免疫反应的进行。
尽管这项策略或许会很难在全球范围内实现,但研究者在开发抵御病毒入侵技术上的努力或许也是人类抵御疾病的一项巨大进展。

应对其它狡猾病原体的好消息
促进机体产生特殊抗体的疫苗往往能够帮助应对其它非常棘手的感染,比如流感病毒,其经常会以不同的结构再度出现来躲避机体在此前感染中已经形成的免疫力;而疟原虫在感染期间也会产生成百上千个靶点,其能够混入到免疫系统中,从而使得机体很难重点关注靶向清除感染的抗体的产生,登革热病毒也能够控制机体免疫系统来为错误的靶点产生抗体,当然同时还会诱发潜在致命的结果。
如今研究者们花费了大量精力来寻找能够克服流感、疟疾、登革热以及丙肝病毒感染的新型抗体技术,为了实现该目标,研究者对成千上万个单一免疫细胞进行筛查来寻找最具潜力的抗体来同时促进多个突变的病原体失去活性,当然研究者也取得了一定进展,近来就有研究人员鉴别出了一种特殊抗体,起能够保护机体抵御四种不同版本的登革热病毒的感染。
障碍是什么?
目前利用这些抗体有两种主要选择,其一就是直接将抗体注射到已经感染一种病原体的患者机体中,另一种则是首先利用疫苗抑制机体感染,或许未来某一天就能够彻底根除疾病。
当然目前在疫苗开发上仍然存在很多困难,在HIV感染期间,最佳的抗体常常需要花费长达一年时间才能够发挥作用效力,而机体对疟疾的获得性免疫则需要多重感染以及很多年才能够获得,这往往会让很多年轻人处于死亡的风险之中,当然研究者也并不清楚是否他们设计的疫苗能够加速患者的治疗过程。
当然机体的免疫力依旧在持续工作,因为在感染损伤机体之前,免疫记忆细胞能够非常快速且更好地抵御感染的发生;但不幸的是,HIV、疟疾和丙肝通常都会消耗机体的免疫记忆细胞,研究者并不清楚是否一种针对HIV的疫苗能够有效制造出更加有效的免疫记忆细胞,或者是否被消耗殆尽的记忆细胞能够阻断疫苗有效发挥作用。
尽管存在很多问题,但在过去十年里科学家们取得的研究进展已经使得他们有可能开发出针对侵入性病原体的新型策略或疗法。(生物谷Bioon.com)
本文系生物谷原创编译整理,欢迎转发,转载需授权!点击 生物谷app.
参考资料:
【1】Articles on HIV
【2】HIV/AIDS
【3】Bound for Glory
Science DOI: 10.1126/science.341.6151.1168
【4】HIV Vaccine Design to Target Germline Precursors of Glycan-Dependent Broadly Neutralizing Antibodies.
Immunity doi: 10.1016/j.immuni.2016.08.016
【5】Sequential Immunization Elicits Broadly Neutralizing Anti-HIV-1 Antibodies in Ig Knockin Mice.
Cell doi: 10.1016/j.cell.2016.07.030
【6】Explainer: how viruses can fool the immune system
【7】Recognition determinants of broadly neutralizing human antibodies against dengue viruses.
Nature doi: 10.1038/nature14130
【8】Antibody injections could be stepping stone to HIV vaccine
【9】How HIV’s evasion tactics could help fight the flu