《自然》子刊:胰腺癌治疗新进展!CXCR4拮抗剂+PD-1抑制剂+化疗的三联疗法,初步试验中疾病控制率达77% | 临床大发现
胰腺癌,也许是免疫治疗最难啃的一块硬骨头。
厚重的细胞外基质作为防护壳,抑制性极强的免疫微环境,加上狡诈多端的癌细胞,此前所向披靡的PD-1抑制剂,也没法上演单骑救主的好戏。
但是我们还有“协同作战”这一招。近期公布的临床试验COMBAT(KEYNOTE-202)的数据显示,新型CXCR4抑制剂BL-8040(Motixafortide),配合PD-1抑制剂和化疗联合使用,在胰腺癌的二线/三线治疗中初步效果良好。
这种三联疗法,在试验中作为二线治疗使用,疾病控制率达到77%,其中35%的患者实现了客观缓解,缓解持续时间达到7.8个月,这些数据都是胰腺癌治疗多年来难得的进步[1]。相关数据发表在《自然·医学》上。
看到Review上的新药出成绩,不错不错
(图片来源:Nature Reviews Clinical Oncology)
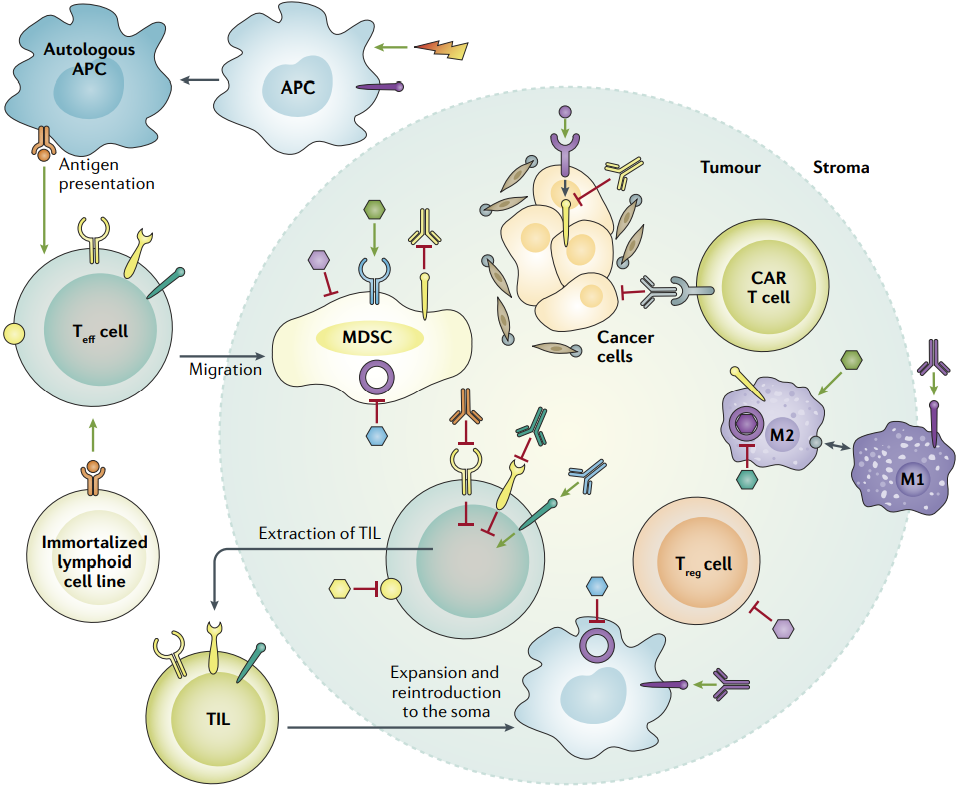
对于胰腺癌为什么难治,科学家们已经总结出了不少原因,其中很重要的一条就是肿瘤微环境当中,CD8+T细胞的数量实在是太少。即使免疫检查点抑制剂能穿越重重屏障抵达肿瘤部位,也很难调动起足够强大的抗肿瘤免疫应答[2]。
所以要想让PD-1抑制剂们具备挑战胰腺癌的能力,就得给它配上可靠的队友。本次试验中使用的CXCR4抑制剂,就是近年来颇受关注的新星,因为很多癌细胞都存在CXCR4的高表达。
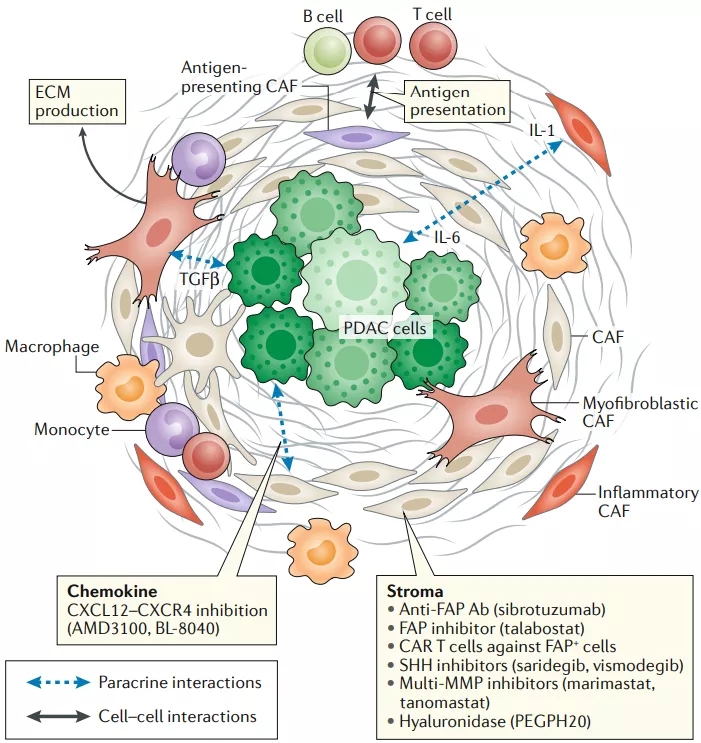
具体到胰腺癌的话,抑制CXCR4一方面可以增加肿瘤微环境中T细胞的数量,同时还可以针对一下胰腺癌细胞外基质中,大量存在的肿瘤相关成纤维细胞(CAF)[3-4]。这样双管齐下,就能削弱胰腺癌肿瘤微环境对于免疫治疗的不利影响。
图上的每一个要素,都可能对免疫治疗效果有影响
(图片来源:Nature Reviews Clinical Oncology)
动物实验也显示,PD-1/L1抑制剂与CXCR4抑制剂联合使用,会存在协作增效性,所以让这两种药物联手,就是非常自然的选择了。
接下来就说说COMBAT试验,这项试验分为两部分进行,第一部分先是验证BL-8040+帕博利珠单抗,作为后线治疗的安全性和初步疗效。在胰腺癌当中,三线和三线以上的治疗难度很大,缺乏成熟的方案。
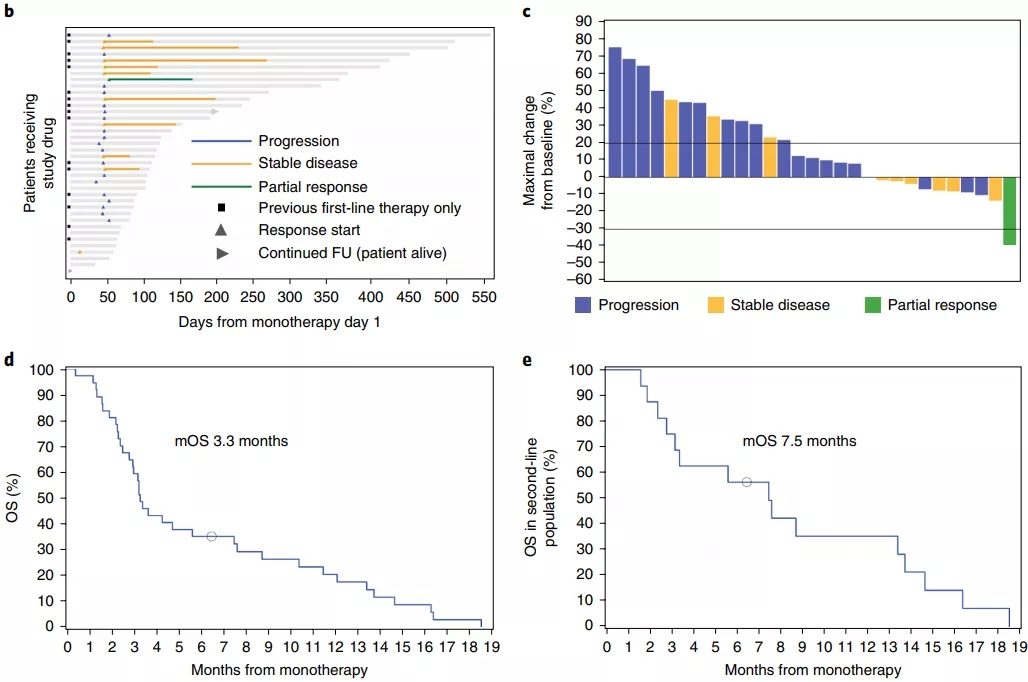
这部分试验总共有29名患者参与,BL-8040+帕博利珠单抗的整体疾病控制率为34.5%,只有一名患者达到客观缓解,这也体现了胰腺癌的“硬骨头”。
但分析数据显示,疗效主要体现在二线治疗的16名患者当中,他们的中位生存期达到7.5个月,明显优于此前FDA批准的伊立替康脂质体+氟尿嘧啶+亚叶酸钙方案的生存期(6.1个月)。
三线及三线以上的患者,把左边的患者整体生存期拉得好低……
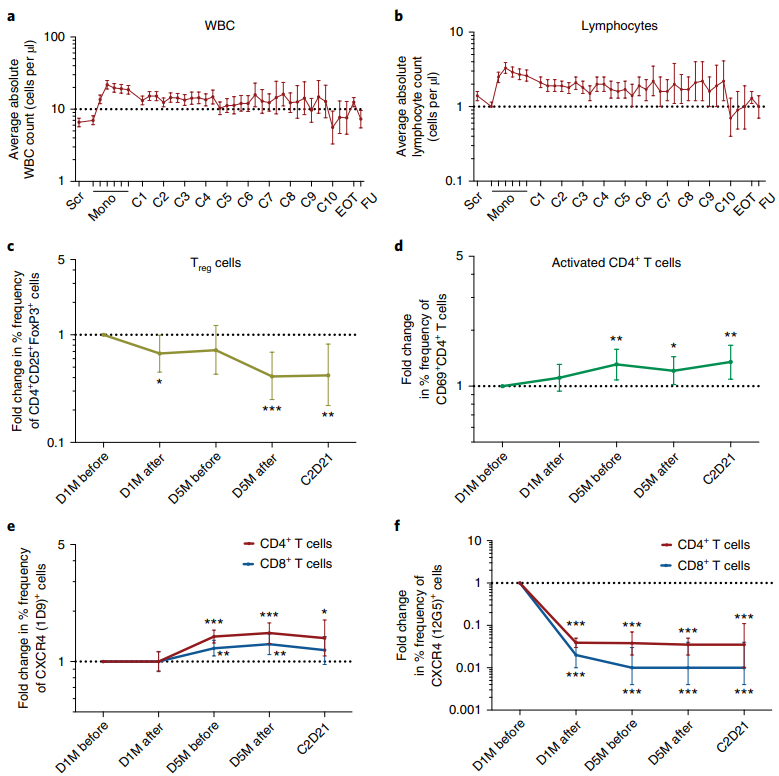
各种检测结果也提示,BL-8040+帕博利珠单抗的治疗,增加了外周血中活化T细胞的水平,减少了调节性T细胞的数量,浸润到肿瘤内的CD8+T细胞也明显增多。
活化T细胞是侧面衡量疗效的手段
基于这些结果,研究团队在试验第2部分专门入组了22名吉西他滨一线治疗后,病情出现进展的转移性胰腺癌患者,在BL-8040+帕博利珠单抗的基础上,加用伊立替康脂质体+氟尿嘧啶+亚叶酸钙的三药化疗方案进行治疗。
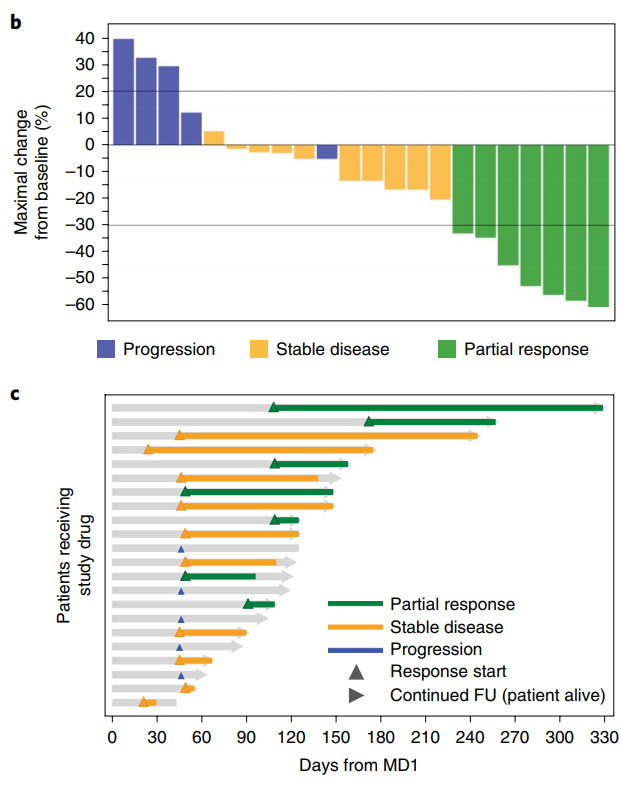
有了化疗强力增援,疗效立马就上去了。22名患者中有7名实现部分缓解,客观缓解率为32%,而中位缓解持续时间达到了7.8个月,明显优于单纯化疗。再算上10名治疗后病情未进展的患者,整体的疾病控制率(DCR),达到了77%!
缓解和疾病控制,持续时间都不差嘛
三药化疗方案在此前的临床III期试验中,客观缓解率和疾病控制率分别是17%和52%[5]。而且这22名患者中并不存在微卫星不稳定性高(MSI-H),更适合免疫治疗的患者,所以BL-8040+帕博利珠单抗提升的疗效就更不易了。
虽然看似用药很多,但22名患者中只有两名因为副作用明显而停药,3-4级的严重不良事件以腹泻和乏力为主,发生率也比较低。因此研究团队认为,治疗方案也是安全可耐受的。
不过在本次论文中,并没有公布试验第2部分的总生存期(OS)、无进展生存期(PFS)等指标。BL-8040和PD-1抑制剂的搭档到底能体现多大价值,就有待后续数据和试验去揭晓啦。
参考资料:
1.Bockorny B, Semenisty V, Macarulla T, et al. BL-8040, a CXCR4 antagonist, in combination with pembrolizumab and chemotherapy for pancreatic cancer: the COMBAT trial [J]. Nature Medicine, 2020.
2.Ho W J, Jaffee E M, Zheng L. The tumour microenvironment in pancreatic cancer — clinical challenges and opportunities [J]. Nature Reviews Clinical Oncology, 2020.
3.Seo Y D, Jiang X, Sullivan K M, et al. Mobilization of CD8+ T cells via CXCR4 blockade facilitates PD-1 checkpoint therapy in human pancreatic cancer[J]. Clinical Cancer Research, 2019, 25(13): 3934-3945.
4.Feig C, Jones J O, Kraman M, et al. Targeting CXCL12 from FAP-expressing carcinoma-associated fibroblasts synergizes with anti–PD-L1 immunotherapy in pancreatic cancer[J]. Proceedings of the National Academy of Sciences, 2013, 110(50): 20212-20217.
5.Wang-Gillam A, Li C P, Bodoky G, et al. Nanoliposomal irinotecan with fluorouracil and folinic acid in metastatic pancreatic cancer after previous gemcitabine-based therapy (NAPOLI-1): a global, randomised, open-label, phase 3 trial[J]. The Lancet, 2016, 387(10018): 545-557.