综述:基因治疗的前世今生(下)
上篇中,医麦客小编为大家介绍了基因疗法的发展历程以及国内对该领域的发展布局;以下,小编将对目前基因疗法领域的技术发展以及现行的相关法规政策进行一个大致的概述。
基因疗法技术的不断突破
(1)腺相关病毒(AAV)载体技术
腺相关病毒(AAV)最早于在20世纪60年代中期从实验室腺病毒(AdV)制剂中发现,随后很快就在人体组织中被发现。它具有无致病性、高效的长期基因表达、易于基因操作以及免疫反应低(或在许多情况下缺乏)的特点,这一系列特性使其成为基因递送的重要工具。
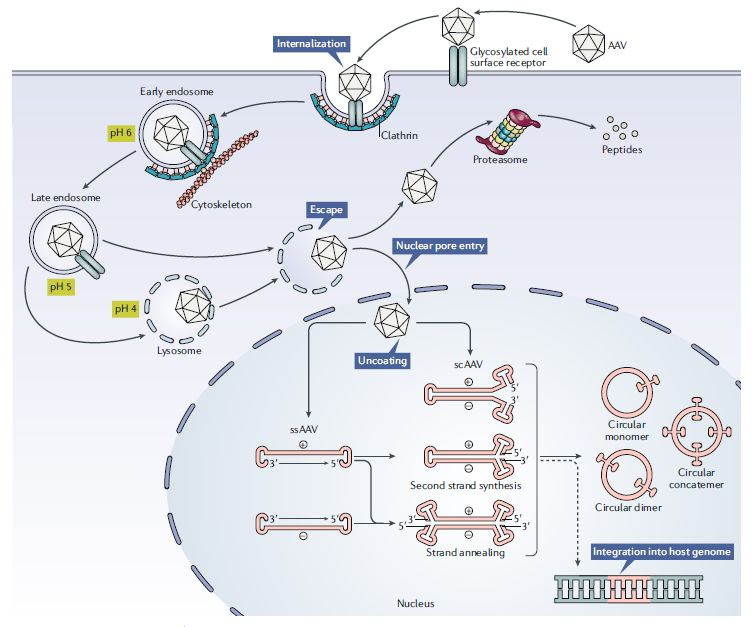
▲重组AAV载体介导转基因表达的过程
目前,最新的AAV基因组设计能够将衣壳中携带的单链DNA设计成自我互补的序列。这种序列的优点在于它不需要单链DNA复制成为双链DNA的步骤就可以进行转录,与传统的单链AAV基因组相比,它的基因表达更为迅速,而且表达量更高。诺华公司开发的治疗脊髓性肌肉萎缩症(SMA)的Zolgensma就使用了这种基因组设计。然而这种设计的一个缺点是AAV携带的转基因容量减半,还需要进一步研究优化。
至今为止,全球已有三款以重组AAV为载体的基因治疗药物获批上市,除了诺华公司的Zolgensma(AAV9)以外,另外两款是UniQure公司开发的Glybera(AAV1)和SparkTherapeutics公司开发的Luxturna(AAV2);另外还有一款治疗A型血友病的AAV基因治疗药物BMN-270(来自BioMarin)也提交了上市申请。由此我们可以看出AAV基因疗法的潜力是巨大的。
(2)CRISPR基因编辑技术
作为基因编辑工具,CRISPR已经成为生物医学领域的最热门技术。早在20世纪下半叶,CRISPR序列就已经被科研人员发现并记录 ,直到2002年,这些序列正式被命名为:规律间隔成簇短回文重复序列(Clustered Regularly Interspaced Short Palindromic Repeats, CRISPR)。
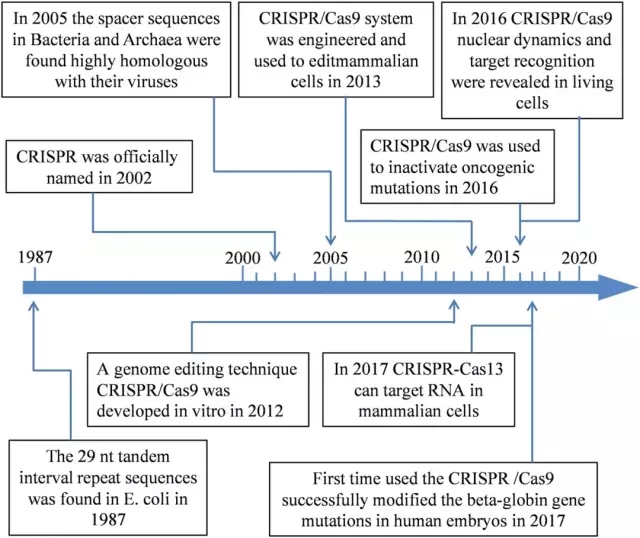
▲ CRISPR技术发展时间轴(图片来源:Nature)
从那时起,研究人员发现CRISPR/Cas9的功能非常多样。科学家不仅可以使用CRISPR通过剪断基因来“沉默”基因,还可以利用修复模板将剪切片段留下的缝隙替换为所需的基因。
随后,科学家们对CRISPR技术进行了多方面的改进研究,截止2017年,关于CRISPR的论文,就已经有超过14,000篇。目前,该技术发展的相当成熟,已经广泛运用于基因疗法领域,有望帮助各类遗传性基因疾病患者获得新的治疗途径。
(3)单/双碱基编辑技术
现有的基因编辑技术,例如CRISPR、ZFN、TALEN,通过在DNA中产生靶向的双链断裂,然后依靠细胞自身修复机制来完成编辑过程;这些方法可以有效地改变基因表达。然而,它们缺乏对编辑结果的控制,脱靶效应以及对DNA双链断裂的依赖,可能导致基因编辑后的细胞出现不可预期的混乱。许多基因组突变发生在单个碱基中,为使基因编辑更加精确,单碱基基因编辑技术应运而生,旨在针对这些单一的碱基错误(即点突变),而不会在DNA中造成双链断裂。
2016年4月,David Liu教授团队在Nature上发表的论文表示,首次开发出了胞嘧啶碱基编辑器(CBE),能够在不依赖DNA双链断裂的情况下首次实现了对单个碱基的定向修改。这便开启了CRISPR系统的单基因编辑时代。随后,David Liu教授团队又开发了另一种单碱基基因编辑工具——腺嘌呤碱基编辑器(ABE),从此研究人员首次实现了不依赖于DNA断裂而能够将DNA四种碱基A、T、G、C进行替换的单碱基基因编辑技术。
但科学家们在随后的研究过程中发现,单碱基编辑系统存在严重的脱靶效应,同时会诱导大量基因突变,另外还存在着编辑窗口单一、编辑转化效率不高等缺点,故而对其展开了一系列的优化改善研究;2019年10月,David Liu团队再次开发出先导编辑器(Prime Editor, PE),一种能够搜索和替换(碱基)的基因编辑器,在不依赖DSB和供体DNA的条件下便可有效实现所有12种碱基转换(C→T、G→A、A→G、T→C、C→A、C→G、G→C、G→T、A→C、A→T、T→A和T→G),此外还能有效实现多碱基的精准插入。
2020年6月,国内邦耀生物与华东师范大学刘明耀教授及李大力教授团队合作的一项研究表明,将胞嘧啶脱氨酶hAID-腺嘌呤脱氨酶-Cas9n(SpCas9 D10A突变体)融合在一起,开发出的一种新型双功能碱基编辑器-命名为:A&C-BEmax,不仅可以实现单独的C>T或A>G,还可以在同一等位基因上同时实现C>T和A>G的高效转换。双碱基基因编辑技术的出现极大地丰富了碱基编辑工具、扩展了碱基编辑器的应用范围,为遗传病治疗、作物育种等于带来新的发展,可以说是人类在基因编辑领域新的突破。
(4)溶瘤病毒基因改造技术
溶瘤病毒(Oncolytic Virus, OV)是一类能选择性感染和杀伤肿瘤细胞的病毒,具有特异性复制能力,并能激发机体产生抗肿瘤免疫反应。它们的作用原理主要是通过对自然界存在的一些致病力较弱的病毒进行基因改造制成特殊的溶瘤病毒,利用靶细胞中抑癌基因的失活或缺陷从而选择性地感染肿瘤细胞,在其内大量复制并最终摧毁肿瘤细胞。
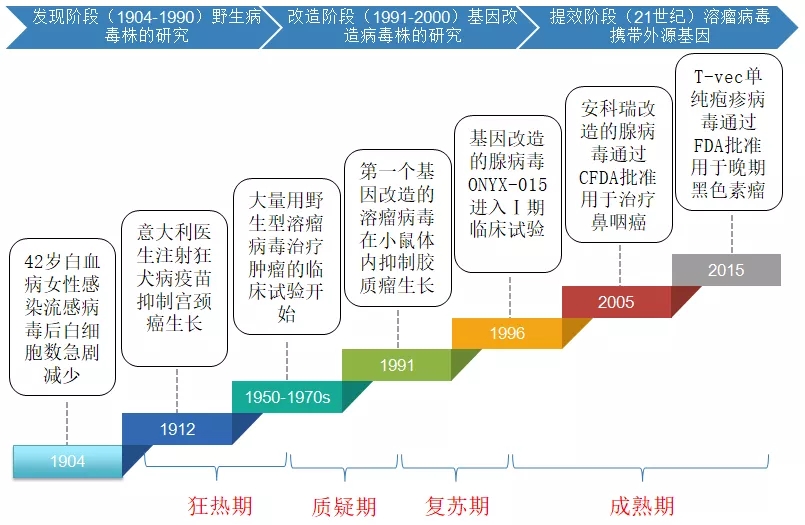
▲ 溶瘤病毒发展史
溶瘤病毒疗法最初发现于20世纪初期,活跃于20世纪中期的大量临床试验,但由于当时技术有限,主要都是利用天然的溶瘤病毒,其引发的强烈免疫反应和并发症导致效果不佳、副作用大,使得当时化疗和放疗显示出了颠覆性的疗效,故而该领域受到冷落。
后来,随着病毒学和基因工程技术的不断发展,使得人们能对病毒基因进行改造,这大大提高了溶瘤病毒在肿瘤治疗方面的效果、特异性和安全性。之后,溶瘤病毒就开启了肿瘤治疗的新纪元——溶瘤病毒疗法。
随着重组病毒基因组改造技术的逐渐成熟,溶瘤病毒疗法技术已广泛运用于实践。其里程碑事件,是2015年美国FDA和欧盟批准溶瘤病毒T-Vec上市;目前T-Vec已在美国、欧洲和澳大利亚广泛用于复发黑色素瘤治疗。近几年,该领域似乎重新回归到大家的视野中,成为国内外基因疗法研发领域的星星之火,值得期待。
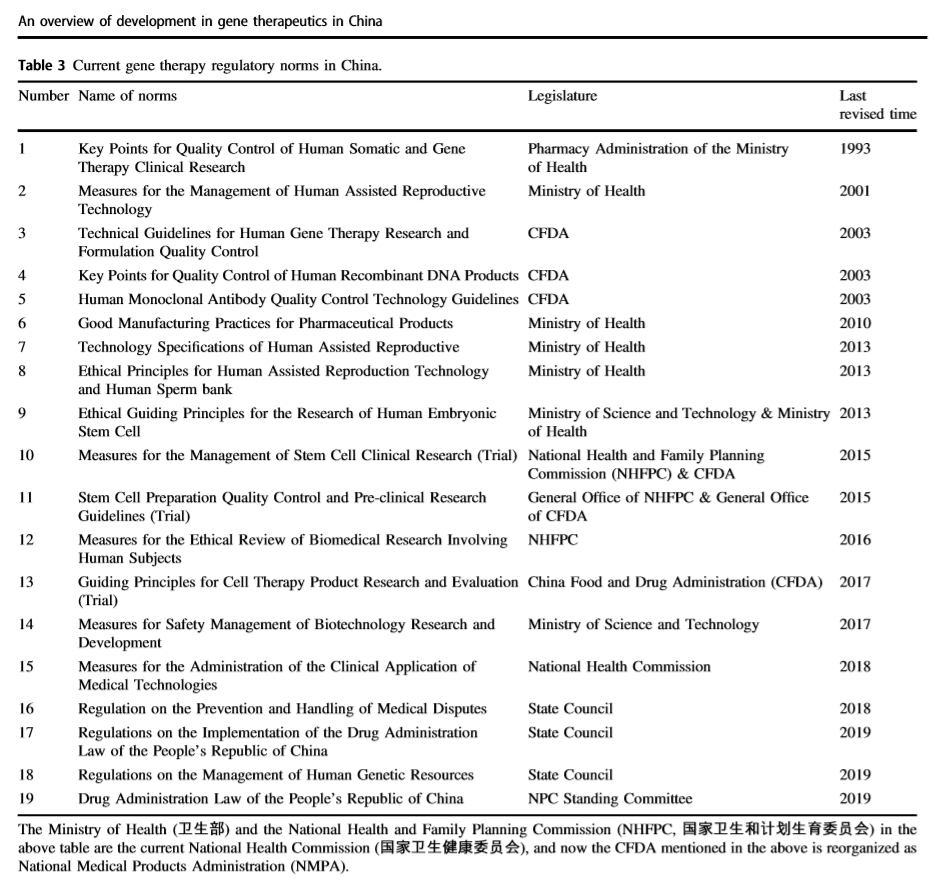
基因疗法监管机制的发展
展望
近年来,我国基因疗法领域正在逐步兴起。作为一种新的医学领域,它正在深刻地改变着制药业的面貌,但还并未发展成熟,对此人类还需要进行更长时间的探索和发现。
尽管如此,这并不可怕。“泡泡男孩”的基因疗法事件告诫我们,相比于恐惧,在学习中探索未知,才会使基因疗法领域得到蓬勃发展,才能使得更多患者获得生的希望。
因此,公众对该领域的认可、国家社会对该领域的支持、相关法律法规的建树,都将会成为该领域新疗法诞生的关键推力。
2020年8月22-23日于上海举办2020溶瘤病毒药物开发论坛(Oncolytic Virus Drug Development Forum 2020)。大会将围绕肿瘤治疗前沿技术及溶瘤病毒产品法规解读、 溶瘤病毒产业转化、溶瘤病毒项目经验分享,以及新型溶瘤病毒的发展及资本支持四个主题,专项技术深耕挖掘,为行业带来前所未有的深度技术交流及成功经验分享。
参考资料:
1.An overview of development in gene therapeutics in China