Cell子刊:王存玉院士发现抗癌新思路,抑制酶活性,提高癌症免疫疗法效果
撰文 | 王聪
编辑 | nagashi
排版 | 水成文
随着生物学和医学的发展,人类对癌症以及自身免疫系统的认知愈渐加深,人类在癌症治疗领域接连取得重大突破,尤其是以PD-1/PD-L1免疫检查点抑制剂为代表的癌症免疫疗法的出现,可以说是彻底改变了癌症治疗格局,为癌症患者带来了生的希望。
然而,有许多癌症患者却无法从癌症免疫疗法中受益,头颈部鳞状细胞癌就是这样,对癌症免疫疗法难以产生良好的反应,因此迫切需要更有效的治疗方法。
近日,加州大学洛杉矶分校(UCLA)王存玉院士团队在 Cell 子刊 Molecular Cell 发表了一项题为:Targeting KDM4A epigenetically activates tumor-cell-intrinsic immunity by inducing DNA replication stress 的研究论文。
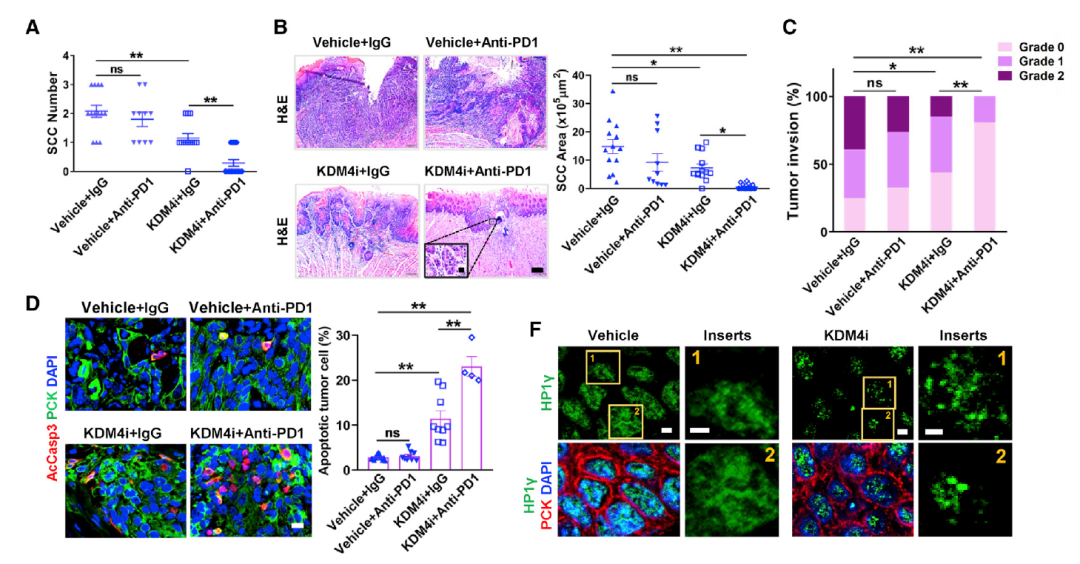
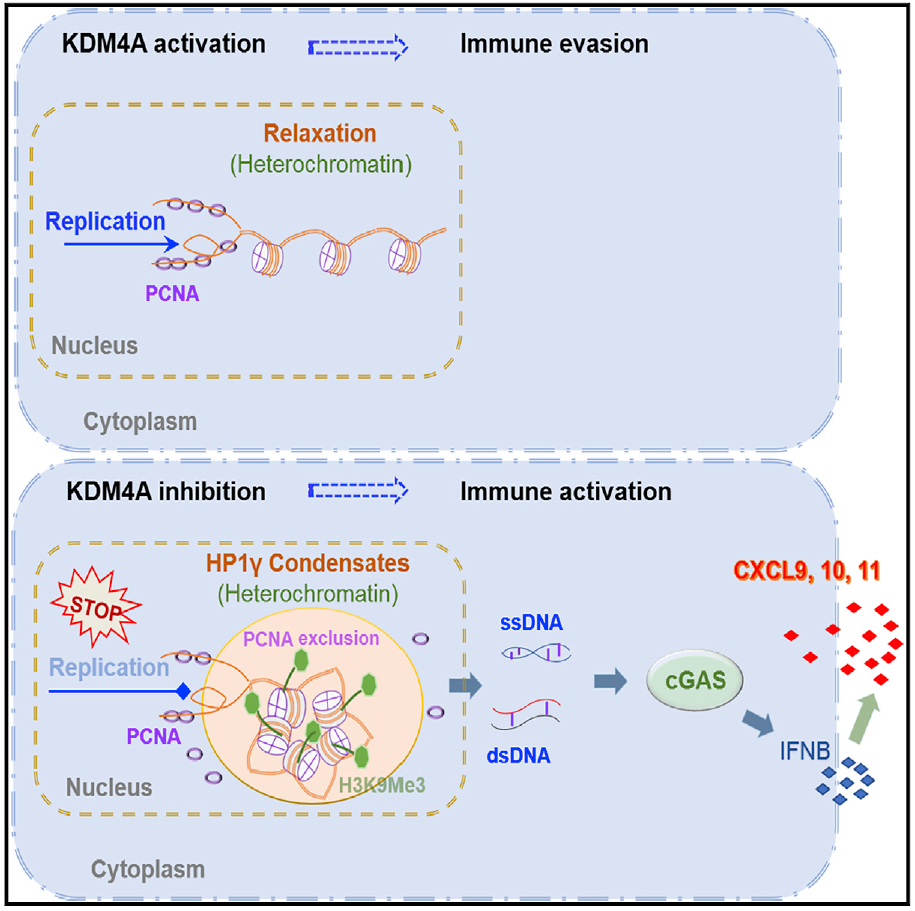
该研究找到了一种能够在头颈癌中起关键作用的酶KDM4A,靶向抑制这种酶,能够通过加重鳞状细胞癌细胞中的复制压力来激活抗肿瘤免疫力,从而改善小鼠模型中的免疫疗法并减缓肿瘤的生长,并增强PD-1抑制剂的免疫治疗效果。
制定激活肿瘤细胞内在免疫反应的策略,利用肿瘤易感性对改善肿瘤免疫疗法至关重要。
KDM4A作为组蛋白H3第9位赖氨酸三甲基化(H3K9me3)脱甲基酶,之前已有研究发现其在鳞状细胞癌的生长和转移中起关键作用。
由于KDM4A的过度表达会促进与癌细胞复制相关的基因表达以及癌细胞在头颈癌的扩散,因此王存玉团队专注于KDM4A在头颈癌中作用和机制的研究。因为已经知道KDM4A基因在癌细胞的复制和扩散中起关键作用,因此王存玉团队将研究重点放在了抑制KDM4A基因上,以确定是否会出现相反的的结果。
研究团队构建了KDM4A基因敲除小鼠模型,通过该模型,研究团队观察到鳞状细胞癌显著减少,并且癌转移至淋巴结的情况也更少。研究团队还发现,KDM4A的敲除还导致抗感染T细胞的募集和激活,从而杀死癌细胞并刺激固有的肿瘤免疫力。
然后,研究团队在另一组小鼠模型中发现,敲除KDM4A基因后,在使用PD-1抑制剂,能够进一步降低鳞状细胞癌的生长和淋巴结转移。
最后,研究团队测试了KDM4A的小分子抑制剂能够提高基于PD-1免疫检查点抑制剂的疗效,实验结果表明,该抑制剂特别有助于清除癌症干细胞。
总的来说,这项研究结果表明,靶向抑制KDM4A,可以通过加重鳞状细胞癌细胞中的复制压力来激活抗肿瘤免疫力,并增强PD-1抑制剂的免疫治疗效果。
这项研究为开发更具KDM4A特异性的抑制剂,开发更有效的挽救生命的癌症疗法具有重要意义。
论文链接:
https://doi.org/10.1016/j.molcel.2021.02.038