国际期刊《Cell》:肿瘤免疫治疗的挑战和方案
嵌合抗原受体(CAR)T细胞疗法是一种新型癌症疗法,该疗法对急慢性白血病有较好效果(70%-90%),但对实体瘤还有待完善。
同时存在一定挑战,主要是需要建立一套可靠、安全、高效率的平台,并且扩大肿瘤种类适用范围,而合成生物学方法在细胞工程的使用,提供了用于免疫细胞规划(programming immune cells)的工具集,这里介绍如何使用这些工具来设计下一代智能T细胞进行精准治疗。
活体细胞治疗方法特点:完成复杂的感知及功能响应
活体治疗方法作为免疫T细胞的重要理念,不同于无生命平台和工具(比如小分子抗体),能够智能感知并进行积极响应的,从而在治疗癌症时发挥极大的功效。
免疫T细胞疗法反映出医药行业多种研究方法的融合
免疫T细胞疗法结合并发挥三种传统治疗方案(抗体,疫苗,移植)的长处,结合系统生物学和细胞工程的相关技术,已成为一个强大而有效的可对抗复杂疾病的细胞诊疗平台
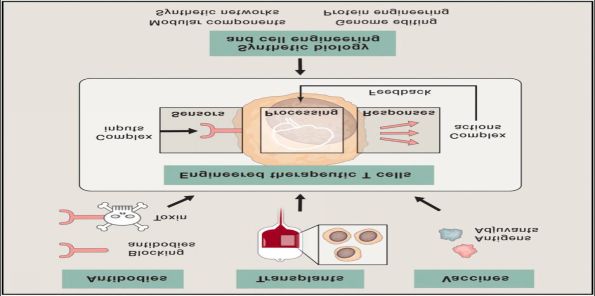
图1:免疫T细胞疗法提供复杂疾病(如癌症)的新的解决平台:疗性的T细胞结合传统治疗方法的元件,集成智能感知和应答剂;同时合成生物学提供免疫治疗细胞编程的工具和方法,来自《Cell》
T细胞疗法临床体验:经验教训
过去20年,T细胞注射疗法的可行性和安全性都得到了证明。开始注射肿瘤浸润性淋巴细胞(TILs)治疗黑色素瘤时,发现T细胞受体(TCR)识别多肽和本体MHC分子(图2A)存在匹配亲和力的问题。经过改进,得到了可多重识别T细胞的分子嵌合抗原受体(CARs)(图2B)。它对常见靶标CD19有着较高的靶向准确率。当然它也存在需要改进的地方,如毒副反应,反应持久性等(图2C)
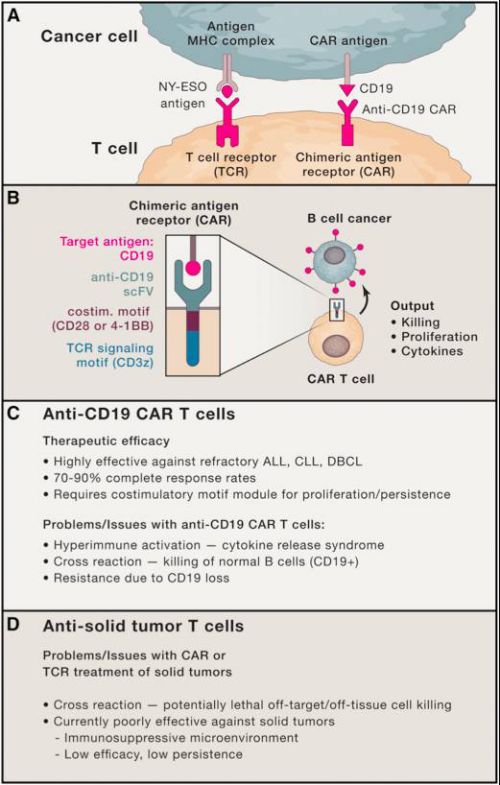
图2:TCR,CAR示意图,来自《Cell》
实体瘤带来的挑战
免疫细胞在肿瘤治疗上最大的挑战是实体瘤。科学家进行了很多尝试(图2D)。如:采用注射携带TCRs或CARs的T细胞来进行免疫治疗;发现了TCR与MAGE家族的强烈交叉毒性反应;对除了CD19的其他靶标(如叶酸受体1α,CD171)的实验等。从中我们得知:
1. T细胞特异性非常重要。
2. 携带TCRs的T细胞毒性很难预测。
3. 会有不可预期的毒副作用。
癌症免疫治疗的多元化挑战和解决方案
针对癌症多维度的挑战,T细胞疗法需具备五项功能来应对
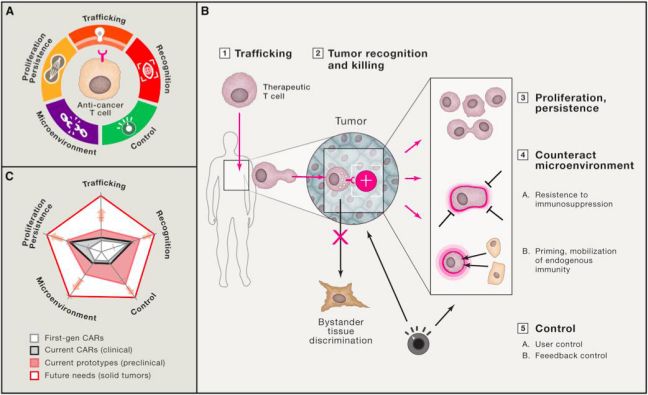
图3:免疫T细胞疗法需要具备的五项功能,来自《Cell》
1.患处的达到 主要针对实体瘤
目前尚无明显进展。
2.病灶的精准识别性
将T细胞识别重定向到指定的抗原,是嵌合抗原受体的核心进展。工程化CAR和TCR提供了重新靶向T细胞的方法,包括它们的活化和它们的细胞毒性作用。
可能的方案:新型的识别受体和系统。例如:“与门线路”-识别结合的多重抗原;“非门线路”-对正常细胞抗原的区别对待;“或门线路”-双抗原靶向CARs;调节亲和性受体等。
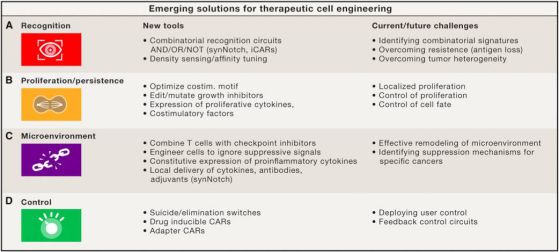
图4:提高细胞免疫疗法的新方案,来自《Cell》
3.细胞增殖与临床效果的持久性(图4B)
有效的细胞增殖是临床疗效的最佳体现。T细胞需要扩展靶向比例,以消除体内肿瘤。 方案:通过多结构域结合、调整T细胞消耗、增强淋巴细胞代谢等,增强细胞增殖。 同时考虑生命周期较长,比如人的生命周期较属的长,p53同种类型调节人类T细胞衰老,但不调节小鼠T细胞。而具有更长端粒的人T细胞亚群更适合过继疗法(adoptive therapy)。
4.抵抗负向微环境(图4C)
特别是对于实体瘤,仅仅关注将T细胞群体靶向肿瘤不足以满足临床疗效,因为许多实体瘤具有免疫抑制微环境。肿瘤产生免疫抑制环境直接下调T细胞的情况下,可能需要额外的工作允许工程化T细胞持续增殖和产生效果。
方案:抑制抗体疗法;“忽视”抑制信号;重塑微环境。
5.控制机制(图4D)
在几乎所有的T细胞临床试验中,都存在严重的不良反应,控制很重要,因为T细胞是自主的 – 一旦它们被转移到患者,就几乎不能做到控制它们。
方案:消灭“开关”;药物控制的“on-swith”CARs;信号调节的CARs;反馈式控制。
免疫细胞疗法与精准医学
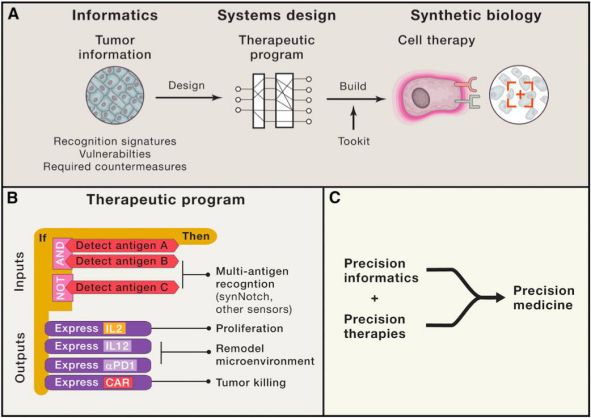
图5:A-免疫细胞疗法;B-系统生物学应用;C-结合精准医学,来自《Cell》
最近几年肿瘤免疫治疗盛行,作为治疗性的T细胞起着主导作用,同时早期的临床经验也暴露出很多挑战,特别是在可靠,安全,有效的平台建立上以及针对实体瘤的局限性。 幸运的是,免疫治疗的兴起与合成生物学和基因组学领域结合,科学家们正在开发有效的工具和方法,以解决T细胞介导的癌症治疗的痛点,工程细胞治疗可能是合成生物学应用的主要的检验平台之一。 免疫细胞治疗也是是精确治疗的主要应用实践之一(图5A)。
我们已经进入了一个不平凡的精准生物信息时代,开始获得关于肿瘤的高度详细的信息 – 哪些抗原存在,哪种类型的抑制分子存在,以及这些是如何分布在组成肿瘤的不同细胞生态系统里(Tirosh et al。,2016)。我们现在有可能使用信息数据来设计优化的治疗反应系统,识别分子特征,攻击肿瘤细胞。我们还可以使用我们新兴的合成生物学工具构建这些系统(图5B)。如果我们能够成功地将精准生物信息与精准细胞治疗相结合,使得这种信息数据的应用方法变得可行(图5C),推动精确医学的概念实现。
最后,虽然我们在这里仅限于使用工程化的免疫细胞来治疗癌症,但是本文讨论的原理也可以用于设计靶向治疗其他疾病的细胞疗法,包括自身免疫,感染,炎症,变性和纤维化等,可以像癌症一样,来接受能够识别和局部应答复的智能细胞治疗的秘密武器。(Fischbach等,2013)。
参考:
1. Cell:The Principles of Engineering Immune Cells to Treat Cancer
2.CD19-targeted T cells rapidly induce molecular remissions in adults with chemotherapy-refractory acute lymphoblastic leukemia. Brentjens, R.J., Davila, M.L. et al. Sci. Transl. Med. 2013; 5: 177ra38
3.Chimeric antigen receptor T cells for sustained remissions in leukemia. Maude, S.L., Frey, N., Shaw, ?et al. N. Engl. J. Med. 2014; 371: 1507–1517
4.CD19 CAR-T cells of defined CD4+:CD8+ composition in adult B cell ALL patients. Turtle, C.J., Hanafi, L.-A. et al. J. Clin. Invest. 2016; 126: 2123–2138
5.T cells with chimeric antigen receptors have potent antitumor effects and can establish memory in patients with advanced leukemia. Kalos, M., Levine, B.L.et al. Transl. Med. 2011; 3: 95ra73