意外发现!疟原虫体内的神奇蛋白竟可对抗 100 多种癌细胞
蛋白质也能治癌症了?前几天, 知名杂志 European Urology 上刊登了一篇文章,研究人员从疟原虫体内分离出一种称为 VAR2CSA 的蛋白质,通过对 VAR2SCA 进行结构改造添加细胞毒性药物,研究人员发现,对药物化疗完全耐药的高度侵袭性膀胱癌小鼠对这种疟疾蛋白质药物组合作出巨大的反应。接受治疗的动物 80% 在 70 天之后仍旧存活,而在三个不同的对照组的其他动物全部死于膀胱癌(1)。
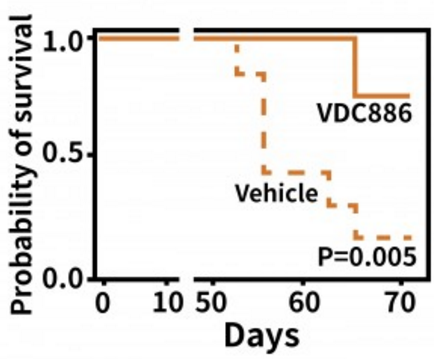
接受 VDC886 治疗动物 80% 在 70 天后存活
众所周知,膀胱癌,是全球第五大常见癌症,由于需要多种治疗方案的介入治疗以及精心的护理,膀胱癌也是目前在每位患者身上花钱最多的癌症。而肌肉浸润性膀胱癌(MIBC)是膀胱癌中最恶劣的一种,5 年生存期只有 50%(2)。尽管过去 20 年外科手术以及系统治疗方案的不断优化,对膀胱癌患者的治疗并没有取得突破进展(3)。目前对 MIBC 的标准治疗方案是基于顺铂的新化疗,然而总受益率也仅 5%-6%(4)。并且只有 40% 左右的患者对新化疗敏感。因此急需新的治疗方案来帮助膀胱癌患者。
温哥华前列腺癌资深研究科学家 Mads Daugaard 说:“这是我们首次将疟疾蛋白质用于癌症治疗的概念直接纳入到临床环境中的研究,大量的临床需求来寻找膀胱癌的新疗法,我们看到有机会用我们新的疟疾药物对抗这种疾病。”所以我们有必要了解一下 VAR2CSA 蛋白以及它治疗癌症的原理。
最初,研究人员发现,在恶性疟原虫传播的地区,人们一般在儿童时期就获得了临床免疫能力,而成年人已经可以逐渐对抗并保护自己免受疟原虫感染。但是孕妇却打破了这一规律,孕妇与其他没有怀孕妇女以及成年男性相比,非常容易感染疟疾并且发病也更严重。妊娠相关疟疾(PAM)的标志性特征是疟原虫聚集在胎盘绒毛间隙,并且造成产妇贫血,早产,新生儿低体重,以及新生儿死亡率的增加(5)。
疟原虫感染的红细胞通过 VAR2SCA 蛋白吸附在胎盘表面
为什么孕妇容易感染疟疾呢?人们发现正常情况下,疟原虫感染红细胞之后容易被脾脏清除,而为了避免被宿主清除,疟原虫在感染红细胞表面产生一种吸附蛋白,集中吸附在胎盘表面。这种吸附蛋白就是 VAR2CSA,介导感染的红细胞吸附到胎盘上特定的糖蛋白,免受宿主清除。这种糖蛋白是一种特定类型称为 CSA 的硫酸软骨素(CS)黏多糖链。因为 CS 在体内其他细胞表面也有表达,但是感染的红细胞仅集中在胎盘表面,表明胎盘表面的 CS 受体 CSA 是一种与其他细胞表面产生的 CS 不同的仅与 VAR2CSA 结合的 CS 亚型(6)。
由于胎盘与癌细胞有一些相似的特征,例如增殖快,具有侵犯性。研究人员设想癌细胞表面会不会也表达与胎盘表面相似类型的 CS 受体。为了验证这一想法,研究人员在体外对 VAR2CSA 蛋白用染色标记重组,用重组 VAR2 蛋白在体外检测人体各组织的正常细胞以及人类癌细胞系。结果发现,VAR2 虽然不与正常细胞结合,但是却和高达 106 种癌细胞相结合占所测试 111 种癌细胞的 95%。并且这一结合可以被纯化的 CSA 阻断,说明多种癌细胞表达与胎盘同类型的 CS 受体(6)。
重组 VAR2 蛋白靶向癌细胞(红色)而对正常细胞不敏感(蓝色)
随后为了验证重组的 VAR2 蛋白是否能被有效利用抑制肿瘤。研究人员将重组 VAR2 蛋白与细胞毒性药物白喉毒素(DT388)融合,创造一种毒蛋白(rVAR2-DT)直接靶向癌细胞抑制其增殖。这种毒蛋白在体外对去势抵抗性前列腺癌小鼠进行实验时发现,仅用 3 剂药物就可以在小鼠体内显著抑制去势抵抗性前列腺癌的生长,并且第一次注射可以在 14 天内持续抑制肿瘤的生长。而正常组织没有任何迹象显示有副反应存在(6)。
但是由于 rVAR2-DT 在人体实验的过程中,高剂量使用时出现了不能良好耐受的副作用,因此,研究人员重新偶联了一种药物 KT886 到重组 VAR2 蛋白上(VDC886)通过重组 VAR2 蛋白将 KT886 运往肿瘤组织产生抑制肿瘤作用,一个重组 VAR 蛋白平均携带 3 个 KT886 药物。并且在小鼠剂量评估中发现,在 15mg/Kg 的剂量下,耐受良好,而且没有显示明显得副作用(6)。之后便重新进行动物模型实验。
在对前列腺癌以及非霍奇金淋巴癌小鼠的治疗中,VDC886 显著抑制肿瘤的生长,并且在治疗的 32 天内 6 只前列腺癌小鼠中 2 只小鼠肿瘤完全消除(6)。
在小鼠的左心室内植入 4T1 转移性乳腺癌细胞,造成强烈的骨转移。接受 VDC886 治疗的 6 只 4T1 骨转移小鼠中 5 只活到了实验结束(54 天)。而对照组全部死亡(6)。
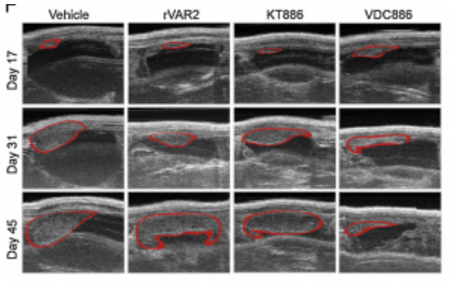
VDC886 治疗小鼠肿瘤生长被抑制对照组肿瘤正常生长 ( 红色表示肿瘤范围)
在对小鼠膀胱癌模型研究中,VDC886 显著抑制对顺铂耐药的小鼠膀胱癌细胞的生长,同时也显著延长了小鼠的生存期,更重要的是,通过组织病理学检查发现 VDC886 没有器官毒性,而且各组小鼠的体重也很稳定。6 只小鼠中 1 只对 VDC886 完全反应,1 只肿瘤显著缩小,另外 4 只肿瘤被稳定抑制。此外,研究人员还发现了一个有趣的现象,对顺铂耐药的小鼠的耐药程度与癌细胞 CS 受体的表达成正相关,即小鼠对顺铂越耐药,小鼠体内表达的癌细胞 CS 受体就越多。这也意味着 VDC886 对化疗耐药的膀胱癌是一种更有效的方法(1)。
总而言之,这些动物实验都证明了一点,即重组 VAR2 蛋白药物偶联物可以靶向多种肿瘤细胞产生的 CS 受体,并对抑制肿瘤生长。因此,这为多种癌症的治疗指明了一个新的方向。目前由 Daugaard 与 Salanti 成立的专注于 VAR2 蛋白对癌症的治疗以及诊断创业公司 VAR2 Pharmaceuticals 正在寻求合作以进行大规模的临床实验。VAR2 蛋白的发现对癌症患者来说又多了一个新的希望。
参考文献:
1.Seiler R, Oo H Z, Tortora D, et al. An Oncofetal Glycosaminoglycan Modification Provides Therapeutic Access to Cisplatin-resistant Bladder Cancer[J]. European Urology, 2017.
2.Madersbacher S, Hochreiter W, Burkhard F, et al. Radical cystectomy for bladder cancer today—a homogeneous series without neoadjuvant therapy. J Clin Oncol 2003;21:690–6.
3.Zehnder P, Studer UE, Skinner EC, et al. Unaltered oncological outcomes of radical cystectomy with extended lymphadenectomy over three decades. BJU Int 2013;112:E51–8.
4.International Collaboration of Trialists, Medical Research Council Advanced Bladder Cancer Working Party, European Organisation for Treatment of Cancer Genito-Urinary Tract Cancer Group, et al. International phase III trial assessing neoadjuvant cisplatin, methotrexate, and vinblastine chemotherapy for muscle-invasive bladder cancer: long-term results of the BA06 30894 trial. J Clin Oncol 2011;29:2171–7.
5.Salanti A, Staalsoe T, Lavstsen T, et al. Selective upregulation of a single distinctly structured var gene in chondroitin sulphate A‐adhering Plasmodium falciparum involved in pregnancy‐associated malaria[J]. Molecular microbiology, 2003, 49(1): 179-191.
6.Salanti A, Clausen T M, Agerbæk M Ø, et al. Targeting human cancer by a glycosaminoglycan binding malaria protein[J]. Cancer cell, 2015, 28(4): 500-514.