解决脑瘤靶向用药 粘性纳米颗粒来帮忙
日前,耶鲁大学(Yale University) 的研究团队在《自然》子刊《Nature Communications》发表论文表明,通过改变纳米颗粒(nanoparticles)表面的化学性质,可以让它们与大脑中的特定细胞相结合。这一发现可能有助于更精确地将纳米药物运送到大脑肿瘤中。
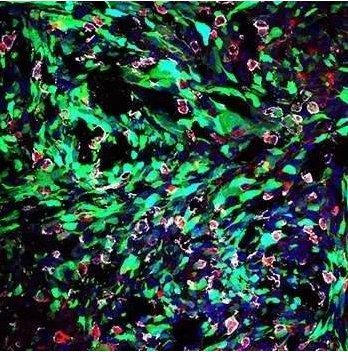
▲纳米颗粒(红色)被小鼠胶质母细胞瘤(绿色)的癌细胞吸收(图片来源:phys.org)
纳米颗粒能够将药物运送到身体特定部位,同时减少药物对正常组织的毒副作用,在治疗癌症和其它疾病方面具有很大潜力。但是,在大脑中使用纳米颗粒目前来说仍然面临着很大的挑战。这一方面是由于血脑屏障(blood-brain barrier)的存在。它导致注射到血循环系统中的纳米颗粒只有不到 1%能够穿越血脑屏障进入大脑。因此,科学家开发出一种称为对流增强运输(convection-enhanced delivery, CED)的方式直接将纳米颗粒通过微创手术注射到大脑组织中,从而绕过血脑屏障的阻碍。为了防止纳米颗粒附着在细胞外基质上并促进它们在大脑组织中的渗透,科学家们在纳米颗粒表面装饰上包括聚乙二醇(polyethylene glycol,PEG)或超支化聚甘油(hyperbranched glycerol,HPG)等不同类型的聚合物。但是即便加上了这些聚合物的修饰,纳米颗粒在治疗大脑疾病的动物模型中的表现仍然不尽人意。那么还有什么因素能够影响到纳米颗粒的生物活性呢?
在这项最新研究中,耶鲁的研究人员把他们的注意力放在注射到大脑组织中的纳米颗粒与不同细胞的相互作用上。当纳米颗粒被注射到大脑组织后,有些纳米颗粒会驻留在细胞间隙(intercellular space)中,而有些纳米颗粒则会通过与细胞膜相互作用,被转移到细胞内部。研究人员发现,根据纳米颗粒表面附着的聚合物的化学性质不同,它们被转移到细胞内部的数量也不一样。表面附着大量 PEG 或 HPG 的纳米颗粒虽然在大脑组织中的渗透能力得到了加强,但是同时它们更不容易被细胞识别并且转移到细胞内部。
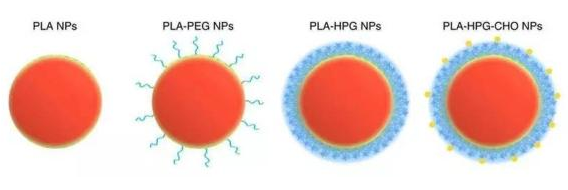
▲具有不同化学表面修饰的纳米颗粒示意图(图片来源:参考资料[2])
对于携带化疗药物的纳米颗粒来说,能够被癌细胞转移到细胞内部可以增强药物的疗效。PEG 和 HPG 修饰本来是为了增强纳米颗粒在大脑组织中渗透能力,现在反而成了降低药效的阻碍。为了让纳米颗粒更容易被转移到细胞内部,研究人员对 HPG 的化学性质进行了改造,他们将 HPG 中的邻位二醇(vicinal diols)转变为醛基(-CHO),这些携带醛基的 HPG(HPG-CHO)更容易与蛋白中的氨基相结合,从而让纳米颗粒变得更容易与细胞发生相互作用。这些具有生物黏附力的纳米颗粒注射到大脑后,能够迅速被大脑中的神经细胞、星形胶质细胞细胞(astrocyte)和小胶质细胞(microglia)转移到细胞内部。大脑中的肿瘤细胞尤其能以很快速度将这些纳米颗粒转移到细胞内部。
为了检验改变纳米颗粒表面的化学性质对纳米药物疗效的影响,研究人员在不同类型的纳米颗粒中装入同样数量的化疗药物,然后将它们注射到携带多发性胶质母细胞瘤 (glioblastoma multiforme) 的小鼠大脑中。他们发现,表面装饰着 HPG-CHO 的纳米颗粒,比表面装饰着 PEG 或 HPG 的纳米颗粒更有效地延长小鼠的生命。
这项研究结果意味着改变纳米颗粒表面的化学性质是调节它们携带的药物在组织中分布的重要手段。研究人员认为未来我们可以通过这一手段改善特定疗法在靶向细胞中的疗效并减少它们对其它细胞的毒性。
参考资料:
[1] 'Sticky' particles promise more precise drug delivery for brain cancer
[2] Surface chemistry governs cellular tropism of nanoparticles in the brain