AZD9291在NSCLC脑转移研究
动物实验证实AZD9291较吉非替尼,阿法替尼等更高
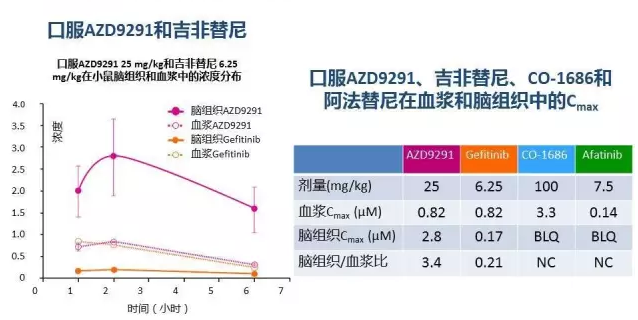
BLQ:低于检测下限;Cmax:最大浓度;CN:未计算
所选择的剂量均在之前的临床研究总报道的临床等效剂量
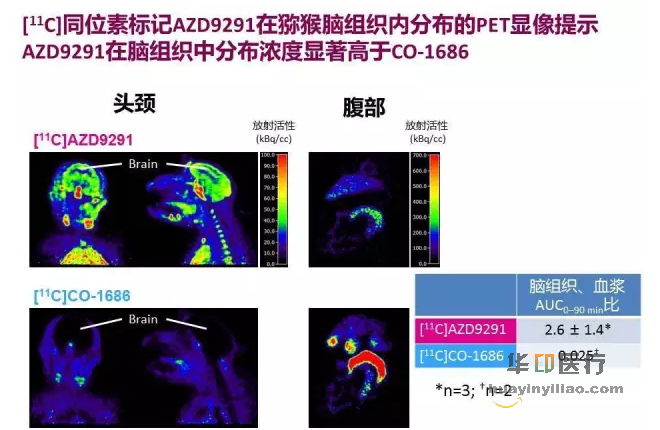
静脉微量注射后5分钟至2小时图像叠加总和
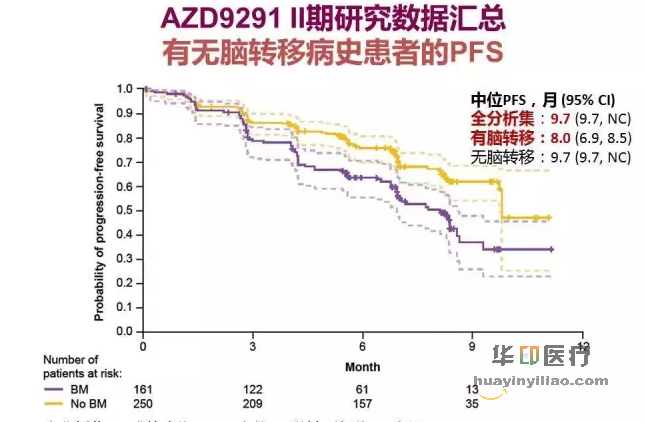
全分析集PFS成熟度为39%,中卫PFS随访时间为6.8个月
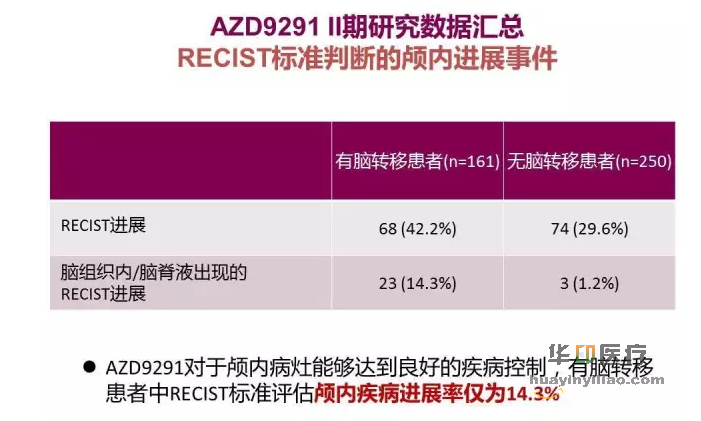
研究结论:
动物实验证实 AZD9291 在脑组织中分布较吉非替尼、CO-1686、阿法替尼更高,并且在小鼠移植 EGFR 敏感突变肺癌脑转移模型中产生显著的肿瘤抑制作用。
AURA II 期扩展与 AURA 2 研究中入组的 39% 无症状稳定脑转移患者中位PFS 8.0 个月,较全分析集人群中位 PFS 9.7 个月相似。
AZD9291 对于颅内病灶能够达到良好的疾病控制,有脑转移患者中 RECIST 标准评估颅内疾病进展率仅为 14.3%。
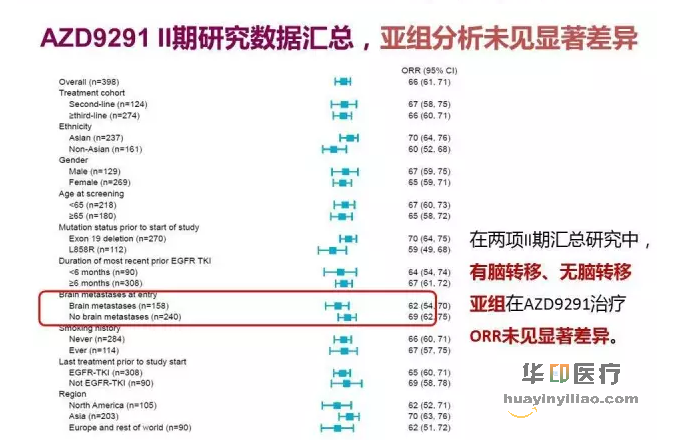
在两项 II 期汇总研究中,有脑转移、无脑转移亚组在 AZD9291 治疗 ORR 未见显著差异。
总 结
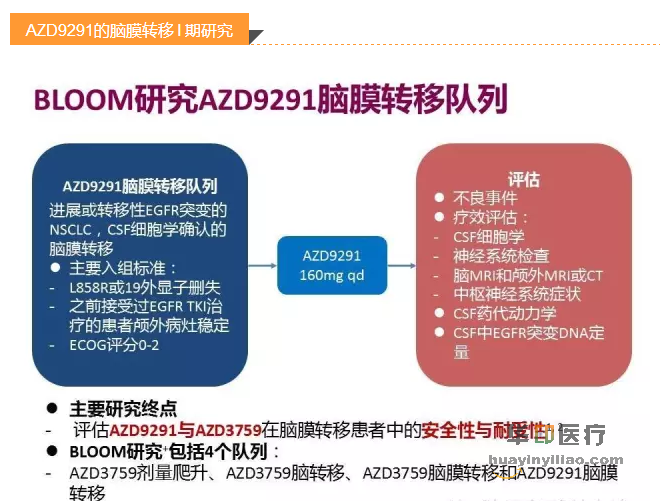
早期数据证实 AZD9291 在既往治疗过的 EGFR 突变晚期 NSCLC 和脑膜转移患者中表现出了可观的疗效。
在这些患者中的疗效提示 AZD9291 能够带来持续的临床获益,大多数患者 4 个月后仍然在接受治疗。
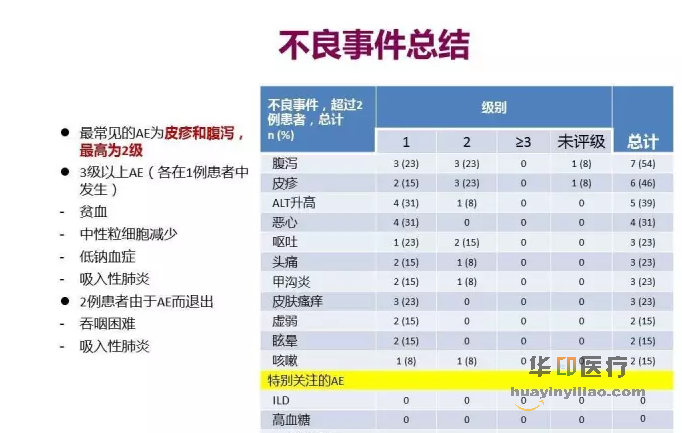
AZD9291 安全性可管理,与既往研究数据一致。

BLQ:低于检测下限;Cmax:最大浓度;CN:未计算
所选择的剂量均在之前的临床研究总报道的临床等效剂量

静脉微量注射后5分钟至2小时图像叠加总和

全分析集PFS成熟度为39%,中卫PFS随访时间为6.8个月


研究结论:
动物实验证实 AZD9291 在脑组织中分布较吉非替尼、CO-1686、阿法替尼更高,并且在小鼠移植 EGFR 敏感突变肺癌脑转移模型中产生显著的肿瘤抑制作用。
AURA II 期扩展与 AURA 2 研究中入组的 39% 无症状稳定脑转移患者中位PFS 8.0 个月,较全分析集人群中位 PFS 9.7 个月相似。
AZD9291 对于颅内病灶能够达到良好的疾病控制,有脑转移患者中 RECIST 标准评估颅内疾病进展率仅为 14.3%。
在两项 II 期汇总研究中,有脑转移、无脑转移亚组在 AZD9291 治疗 ORR 未见显著差异。


总 结
早期数据证实 AZD9291 在既往治疗过的 EGFR 突变晚期 NSCLC 和脑膜转移患者中表现出了可观的疗效。
在这些患者中的疗效提示 AZD9291 能够带来持续的临床获益,大多数患者 4 个月后仍然在接受治疗。
AZD9291 安全性可管理,与既往研究数据一致。