组织驻留记忆T细胞(tissue- resident memory T Cell,TRM))
组织驻留记忆T细胞(tissue- resident memory T (TRM) )是一个特殊的肿瘤浸润淋巴细胞(TIL)亚群,能够无限期地驻留在组织中,并能够对其同源抗原作出快速的免疫反应的TIL。
CD103(整合素αe)是TRM细胞的识别标志,在大多数研究中发现与CD69和/或PD-1的共同表达。肿瘤中TRM细胞的存在与乳腺癌、黑色素瘤患,肺癌,卵巢癌,头颈部鳞状细胞癌,宫颈癌,子宫内膜腺癌,结肠癌,膀胱癌,或胰腺癌无病生存(Disease-Free Survival,DFS)和/或总生存率(Overall Survival,OS)的改善有关。
CD8TRM细胞不存在于循环系统中,而是稳定广泛地存在于人类和小鼠组织中。最初在皮肤和肠道中被鉴定,主要表面marker:CD103和CD69。CD69是T细胞活化的标志,在T细胞受体(TCR)连接1小时内可检测到,下调S1PR1表达,降低S1PR的作用,降低淋巴细胞从组织流出。
CD103和整合素β7形成E-钙粘蛋白的异二聚体受体,在上皮肿瘤细胞和非恶性上皮细胞上表达。因此,CD103TRM细胞粘附在上皮组织上,这有助于它们在外周组织中的保留。但是CD103也表达其他CD4+T细胞,循环T细胞可以在细胞因子或TCR刺激后表达CD69。因此,仅仅依靠CD103和/或CD69的表达来鉴定CD8T RM细胞可能不准确。
与耗竭T细胞(Tex)细胞相似,TRM效应表型的细胞虽然表达高水平的免疫检查点蛋白;然而,不同之处在于,当重新暴露于适当的抗原时,TRM会恢复很强的免疫功能。与非TRM细胞相比,Tim-3+PD-1+TRM细胞具有克隆扩展,富集,细胞增殖和细胞毒性相关的基因转录本。
因而单凭某些免疫检查点表达而将一种状态描述为“衰竭”可能过于简单,不能准确的反应细胞的实际状态。
从黑色素瘤患者中分离出的CD103 CD39TILs具有肿瘤抗原特异性,能够杀死自体肿瘤细胞并分泌IFNγ。这些细胞的较高频率也与头颈部鳞状细胞癌(HNSCC)患者更好的OS有关,TRM细胞表达CD49A,这也表达于从非小细胞肺癌患者组织样本中获得的TRM细胞上。
在另一项研究中,从非小细胞肺癌或结直肠癌患者的肿瘤材料中分离出的肿瘤特异性T细胞,被发现为CD39+,而CD8+CD39-则识别出与癌症无关的表位,并被称为“旁观者”T细胞。
T细胞如何分化为TRM细胞,可能会告知这些细胞可以用来治疗的方法。效应CD8T细胞具有不同水平的KLRG1和IL-7Rα,其中一部分细胞能够下调KLRG1并分化为记忆T细胞。
与KLRG1引起的记忆CD8T细胞相比,下调KLRG1的效应CD8T细胞具有更高−细胞毒性潜能。
TRM细胞可由TGF-β、IL-15、TNF和IL-33等细胞因子调节,而TGF-β细胞可诱导CD103在CD8T细胞上的表达。在转移性黑色素瘤患者中观察到的局部IL-15表达与CD103TRM细胞数增加呈正相关,因此作者认为IL-15影响CD103TRM细胞的保留,尽管这种细胞因子的确切作用尚不清楚。
在乳腺肿瘤标本中已经报道了高水平的TGF-β和TNF,虽然这些细胞因子可能有利于TRM细胞的调节和维持,但没有数据表明这些是TRM细胞在这些细胞因子下分化的关键线索,可能是位置依赖性的。
研究人员已经探索和操纵免疫细胞代谢,试图改善免疫治疗方法,以治疗癌症患者。虽然TRM细胞代谢的临床意义仍有待直接阐明,但已知CD8 TILs能适应肿瘤微环境(TME)中低水平的氧和葡萄糖的代谢。病毒感染产生的皮肤TRM细胞利用外源性游离脂肪酸而不是葡萄糖来维持其寿命和免疫功能 。因此,从脂肪酸氧化获得能量的能力可以为TRM细胞提供在敌对TME中的代谢优势,而TME通常具有较低的葡萄糖水平。
有必要进一步的研究,以确定TRM细胞在乳腺癌中的代谢特性,并了解代谢是否操纵以增强TRM功能,从而有可能揭示新的治疗方法。
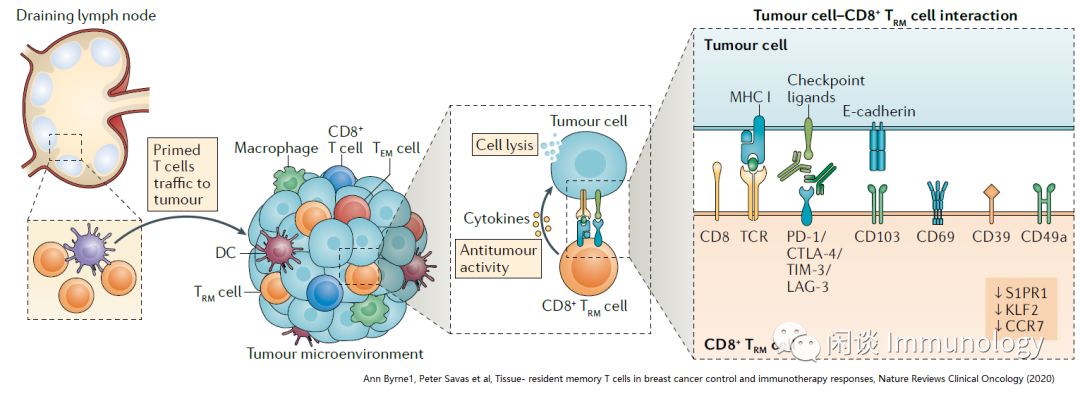
在主要组织相容性复合物I(MHCI)分子的背景下,T细胞由专业抗原呈递树突状细胞(DCS)在引流淋巴结中致敏。
前体记忆T细胞在促炎细胞因子(如I型干扰素)的影响下,进入肿瘤部位并进一步成熟。一群记忆前体细胞将进一步分化为CD103 CD69组织驻留记忆T(TRM)细胞。
与位于肿瘤微环境中的其他T细胞不同,TRM细胞保留在肿瘤组织中,不再循环。CD103与上皮细胞E-钙粘蛋白结合有助于驻留。
活化的TRM细胞具有识别肿瘤细胞表面表达的肿瘤相关抗原(TAAs)、分泌促炎细胞因子和释放能够杀死靶肿瘤细胞的细胞毒性颗粒。
TRM细胞表达高水平的免疫检查点蛋白,如PD-1、CTLA-4、Tim-3和LAG-3,这表明这些细胞也可能对免疫检查点的抑制作出反应。
CD8TRM细胞可以作为免疫检查点抑制反应的生物标志物。CD8TRM细胞上几种免疫检查点蛋白的高表达,提高了它们作为免疫检查点抑制剂的靶细胞群体的可能性。
在KEYNOTE-086试验中获得的样本分析,该试验评估了pembrolizumab治疗转移性TNBC患者的疗效,表明用CD8TRM细胞特征性富集,是对治疗反应预测的有效标志物。一些基因panel可以用于预测肿瘤对于免疫检查点抑制剂的响应。
乳腺癌患者,特别是晚期乳腺癌患者,通常对PD-1/PD-L1抗体没有反应。然后,atezolizumab(商品名 Tecentriq )针对TNBC的三期临床研究(IMpassion130研究),获得阳性结果,导致FDA于2019年3月加速批准抗PD-L1抗体atezolizumab(联合Nabpaclitaxel)治疗晚期TNBC,这是第一次获批乳腺癌适应症。
接受atezolizumab联合Nabpaclitaxel的患者比接受安慰剂加Nabpaclitaxel的患者具有更长的数值中位OS持续时间(中位OS21.0个月与18.7个月;HR0.86,95%Ci0.72-1.02;p=0.078)。然而,atezolizumab益处在很大程度上仅限于这个队列的少数患者(40%),患者≥了1%的PD-L1阳性TILs(使用VentanaSP142分析评估)。
其他免疫治疗策略,如过继细胞治疗(ACT),正在进行很多项实体瘤的研究。假设T细胞激活后,诱导分化为TRM表型可能提供某些优势,使T细胞定位,保留和长期持续。然而,在这种方法成为现实之前,需要更好地理解产生和维持活化的TRM细胞所需的组织特异性因素的特征和作用。
CD39的表达可能有助于鉴定肿瘤特异性CD8TRM细胞。此外,黑色素瘤临床前研究的数据表明,靶向CD39联合免疫检查点抑制剂是增强抗肿瘤免疫的有效治疗策略。CD39在来自乳腺癌患者肿瘤材料的TRM细胞上表达;因此,类似的治疗组合可能在这方面有益处。
喵评:TRM确实独特,带有免疫检查点,但又不同于耗竭T细胞(Tex),遇到抗原又立刻活过来了。对于肿瘤免疫治疗,无论作为预测标志物,还是靶细胞,都有点意思......
参考文献
-
Wang, Z. Q. et al. CD103 and intratumoral immune response in breast cancer. Clin. Cancer Res. 22, 6290–6297 (2016).
Edwards, J. et al. CD103+ tumor- resident CD8+ T cells are associated with improved survival in immunotherapy- naive melanoma patients and expand significantly during anti- PD-1 treatment. Clin. Cancer Res. 24, 3036–3045 (2018).
-
Masopust, D. & Soerens, A. G. Tissue- resident T cells and other resident leukocytes. Annu. Rev. Immunol. 37, 521–546 (2019).
-
Cyster, J. G. & Schwab, S. R. Sphingosine-1- phosphate and lymphocyte egress from lymphoid organs.Annu. Rev. Immunol. 30, 69–94 (2012).
-
Ann Byrne1, Peter Savas et al, Tissue- resident memory T cells in breast cancer control and immunotherapy responses, Nature Reviews Clinical Oncology (2020)
-
Duhen, T. et al. Co- expression of CD39 and CD103 identifies tumor- reactive CD8 T cells in human solid tumors. Nat. Commun. 9, 2724 (2018).
-
Schmid, P. et al. Atezolizumab plus nab- paclitaxel as first- line treatment for unresectable, locally advanced or metastatic triple- negative breast cancer (IMpassion130): updated efficacy results from a randomised, double- blind, placebo- controlled, phase 3 trial. Lancet Oncol. 21, 44–59 (2020).