Nature:27个抗癌「潜力靶点」
免疫疗法已成为癌症治疗的新支柱。近来,越来越多的研究显示,肿瘤内在的代谢程序与免疫疗法的疗效有关。例如,有报道称,黑色素瘤细胞糖酵解代谢的增加与其对过继T细胞疗法以及检查点阻断治疗耐药有关。
细胞代谢是癌细胞和免疫细胞生存能力和功能的关键决定因素。为了维持巨大的合成代谢需求,肿瘤采用了一种特殊的代谢机制,使得其微环境通常是酸性的、缺氧和/或缺乏免疫细胞所需关键营养物质的。因此,事实上,肿瘤代谢本身就是一个能够限制抗肿瘤免疫反应的检查点。
来源:Nature Reviews Cancer
7月6日,最新发表于Nature Reviews Cancer 上的一篇综述中,来自美国约翰斯·霍普金斯大学的两位科学家详细讨论了1)究竟哪些代谢程序对参与免疫反应的特定细胞的功能至关重要?2)这些代谢程序又是如何被肿瘤微环境打乱的?3)这种代谢紊乱是如何影响现有的免疫治疗方法的?4)应如何通过靶向代谢来增强抗肿瘤免疫反应?等问题。文章指出,理解参与抗癌免疫反应的各类细胞的不同代谢需求为选择性调节免疫细胞的功能提供了机会,由此衍生出的新疗法有望成为增强免疫疗法疗效的一种选择。
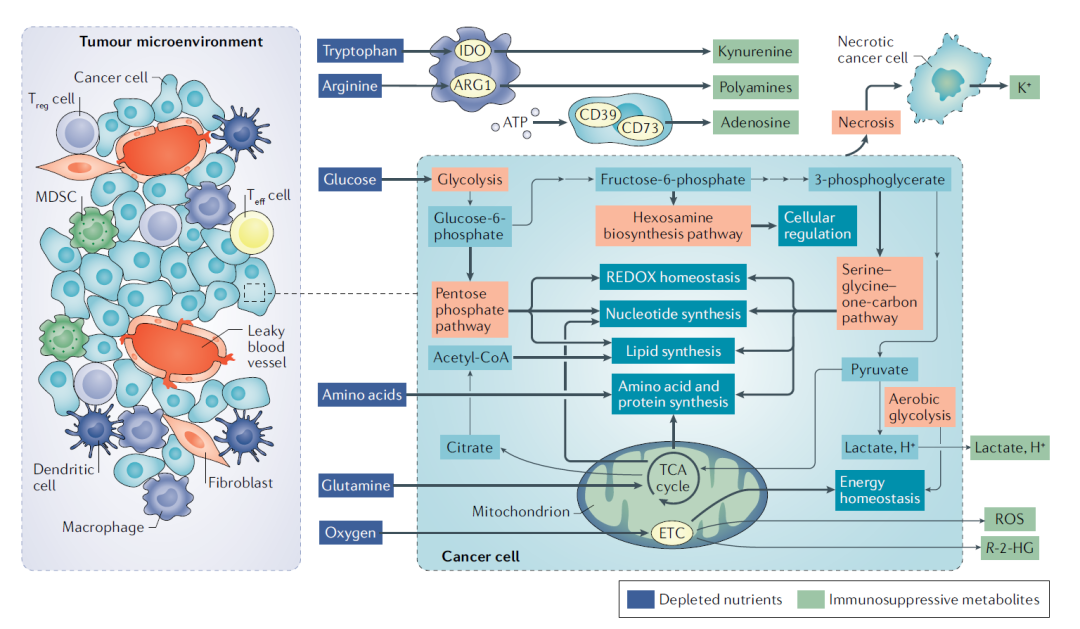
一、肿瘤微环境中的癌细胞代谢
如上图所示,代谢高度活跃的癌细胞对肿瘤微环境产生了深远的影响,导致了营养耗竭、缺氧、酸性环境以及在一定浓度下会产生毒性的代谢物的产生。这对免疫反应有重要影响。不仅缺乏营养和缺氧的微环境会使癌细胞与浸润性免疫细胞之间建立代谢竞争,某些代谢物毒性浓度的产生(如腺苷、犬尿氨酸、鸟氨酸、活性氧和钾水平升高,以及酸中毒增加)也会大大抑制抗肿瘤免疫反应。
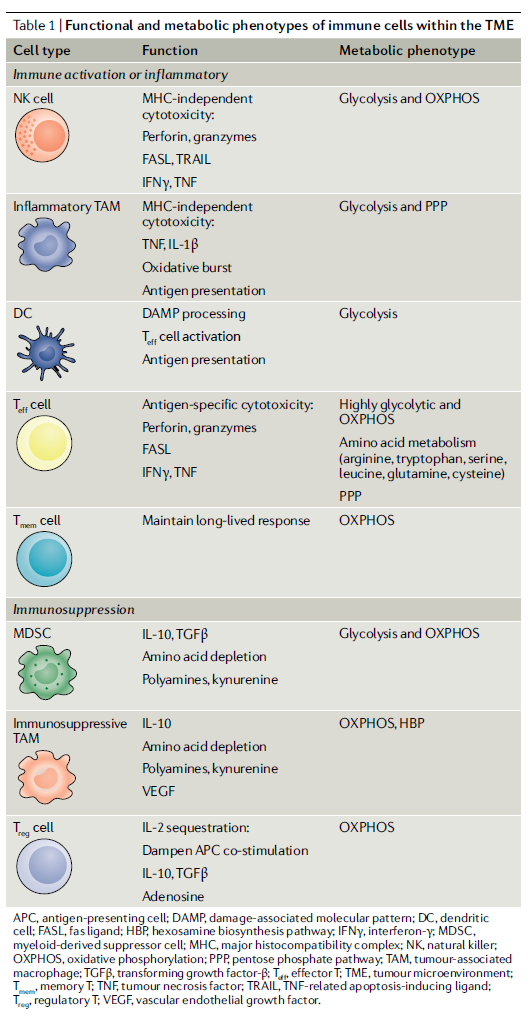
二、肿瘤微环境中免疫细胞的功能和代谢表型
下表总结了肿瘤微环境中的免疫细胞类型。其中,效应细胞执行杀伤功能,既可以来自先天免疫系统,也可以来自适应性免疫系统。来自后者的抗肿瘤效应细胞包括CD4+和CD8+Teff细胞。CD8+Teff细胞在通过诱导细胞凋亡和细胞因子分泌直接杀死肿瘤细胞方面至关重要。CD4+T细胞包括许多亚群。这些亚群中的一些也可以提供显著的抗肿瘤活性,其中研究最透彻的是T helper 1 (TH1)亚群。不同于免疫抑制性促瘤CD4+T细胞(即调节性T (Treg)细胞),这些抗肿瘤的CD4+T细胞统称为常规CD4+ (CD4+conv) T细胞。虽然CD4+convT细胞可能参与直接的肿瘤细胞杀伤,但它们主要通过细胞因子分泌和协助CD8+T细胞激活来促进抗肿瘤免疫。抗肿瘤CD4+convT细胞与CD8+Teff细胞共享着重要的代谢特征。
B细胞也可能在肿瘤微环境中发挥效应作用。重要的是,作为适应性免疫系统的一部分,T细胞和B细胞可以产生记忆细胞群,在感染或肿瘤反应消失后,记忆细胞群可以长期存在。CD8+记忆T (Tmem)细胞是肿瘤长期控制的一个重要方面。
先天细胞,如自然杀伤细胞(NK)和炎性巨噬细胞,也发挥重要的抗肿瘤效应功能。
肿瘤微环境中还存在免疫抑制性细胞群,包括CD4+FOXP3+Treg细胞、骨髓来源的抑制性细胞(MDSCs)、抗炎巨噬细胞和部分B细胞群。通过多种机制,包括分泌细胞因子和代谢紊乱,这些细胞能够抑制或消除抗肿瘤效应细胞群的作用。
最后,抗原呈递细胞,如瘤内树突状细胞(DCs),已被证明在维持肿瘤微环境内的活跃适应性免疫反应方面发挥重要作用。
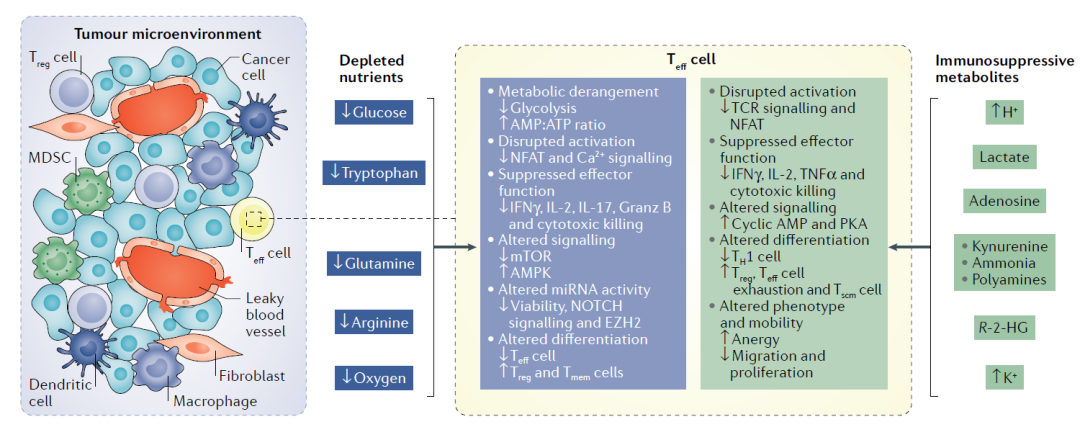
三、肿瘤微环境代谢紊乱抑制T细胞功能
癌细胞代谢产生的许多物质会影响浸润T细胞。举例来说,大量研究显示,肿瘤微环境中细胞外乳酸和H+水平升高可抑制T细胞的增殖、存活、细胞毒性和细胞因子的产生。肿瘤内特定氨基酸(如犬尿氨酸)的积累也会抑制Teff细胞的反应。癌细胞也被报道通过释放肿瘤代谢物(R)-2-羟基戊二酸(R-2-HG)抑制T细胞活性。肿瘤微环境内钾水平的增加也会限制T细胞的效应功能。这些研究突出了肿瘤微环境内癌症代谢产物与免疫功能之间复杂的相互作用(图2)。
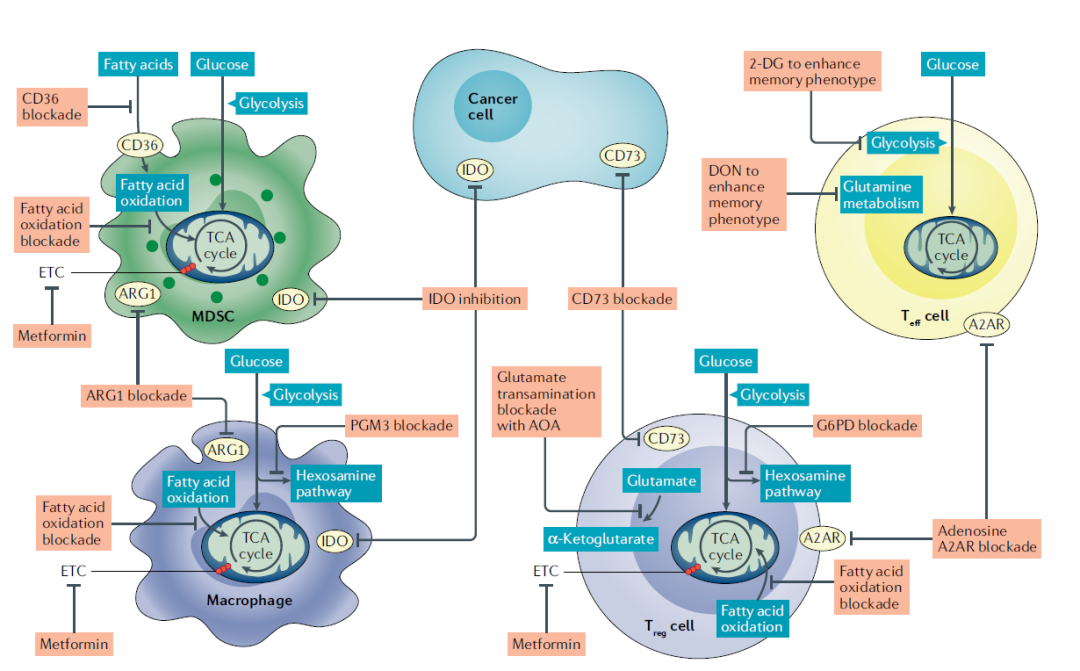
四、27个能够增强抗癌免疫反应的潜在代谢靶点
利用小分子、抗体和基因编辑靶向代谢过程既可用于抑制癌细胞和抑制性免疫细胞的代谢,也可用于支持效应细胞的代谢。抑制性免疫细胞群和癌症中的代谢程序可被靶向以使它们消耗营养物质、导致有毒代谢物或诱导对效应细胞群代谢控制的代谢途径失效。对于效应细胞群来说,代谢干预可能会诱导有益的改变,如延长寿命和抗原特异性免疫记忆。图3及表2总结了增强抗癌免疫反应的潜在代谢靶点。
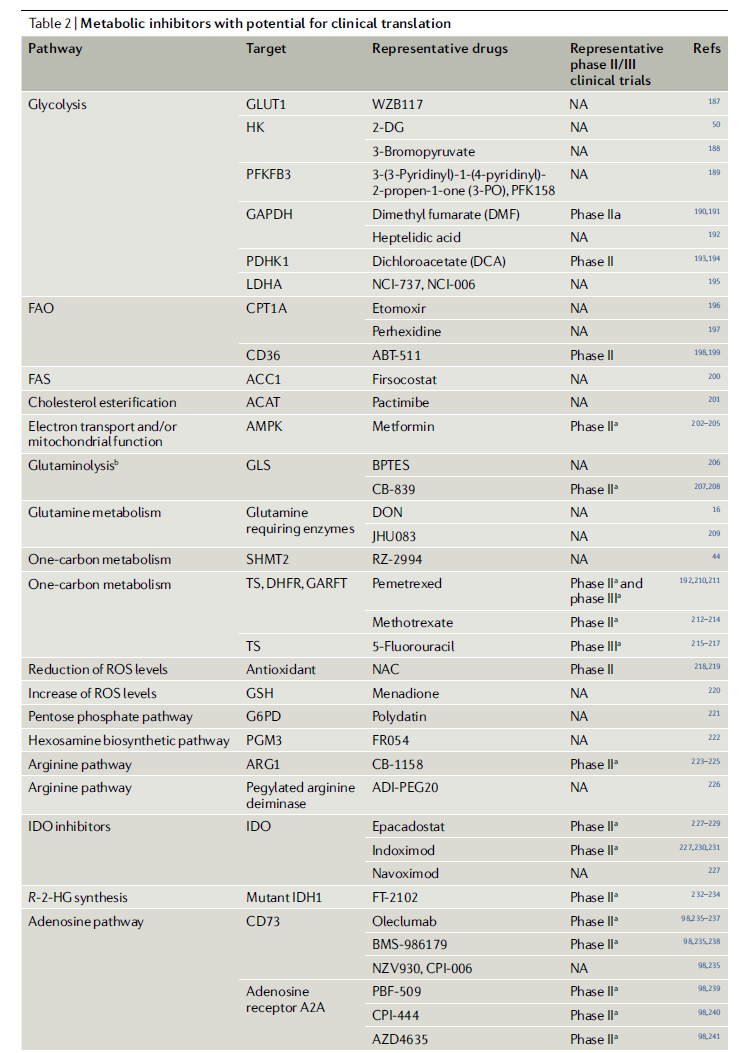
五、38个具有临床转化潜力的代谢抑制剂
大量研究显示,检查点信号可调节肿瘤微环境中的代谢。例如癌细胞上PD-L1的表达能够驱动Akt-mTOR的激活和糖酵解,增加癌细胞与T细胞对葡萄糖的竞争。来自人胃癌组织的T细胞中CD155-TIGIT的信号传导抑制了葡萄糖的摄取、乳酸的产生和糖酵解酶GLUT1和HK2的表达。相反,激活共刺激通路GITR可明显增强T细胞的代谢活性和增殖。此外,在体外研究中,活化的人类T细胞中PD-1和CTLA-4信号传导也会抑制与T细胞激活相关的代谢通路(如有氧糖酵解)。这些发现表明,将代谢抑制剂与检查点抑制剂联合使用有望提高检查点阻断疗法的疗效。下表总结了具有临床转化潜力的代谢抑制剂,共涉及38款代表性候选药物,27个药物靶点。
表2
六、总结
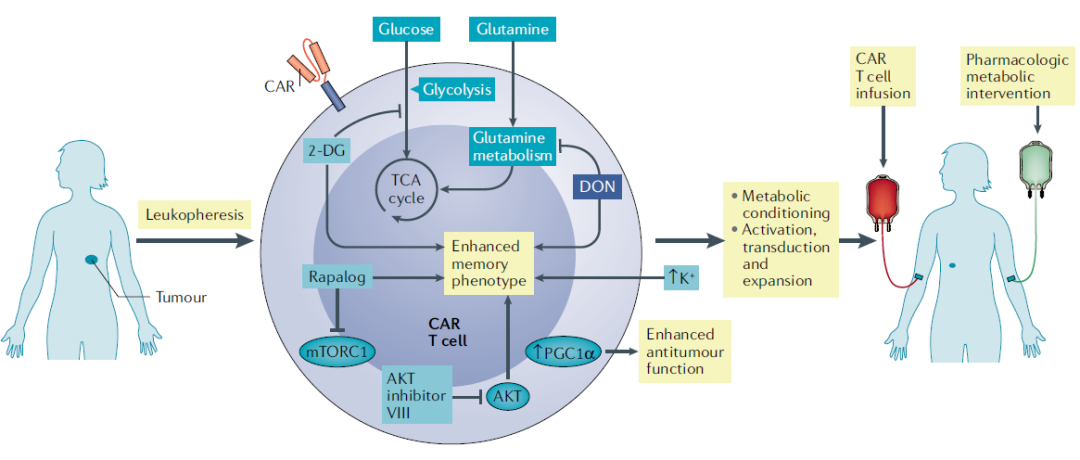
该综述的作者们在结论部分指出,很显然,癌细胞和免疫细胞代谢重编程有明显的区别,对这些区别的认识为通过靶向代谢来增强免疫疗法的疗效提供了新的机会,且这种机会有望通过多种不同的策略来实现,如通过靶向肿瘤的代谢程序来抑制其生长,调节肿瘤微环境;通过靶向抑制性免疫细胞的代谢来抑制这类细胞的功能;通过靶向效应细胞的代谢来增强肿瘤杀伤。值得一提的是,除了将代谢调控与检查点阻断疗法联合,对于过继T细胞疗法来说,对T细胞代谢途径的体外药物或基因重编程也为增强这类疗法的疗效提供了一种手段(下图)。
参考资料: