安罗替尼竟然对TP53突变患者有疗效?!多个案例PR疗效,或成就P53突变治疗突破!
药物背景介绍
安罗替尼是一种新型的口服多靶点抗血管生成酪氨酸激酶抑制剂,在中国已被批准用于晚期非小细胞肺癌的三线和小细胞肺癌的三线治疗。除此,在肉瘤、甲状腺癌、肝癌、乳腺癌、妇瘤等多个癌种中都有数据。依靠抗血管和抑制肿瘤生长的多靶点治疗机制,成为了很多癌种后线的治疗选择。也是化疗、靶向以及免疫的好搭档。
案例分享
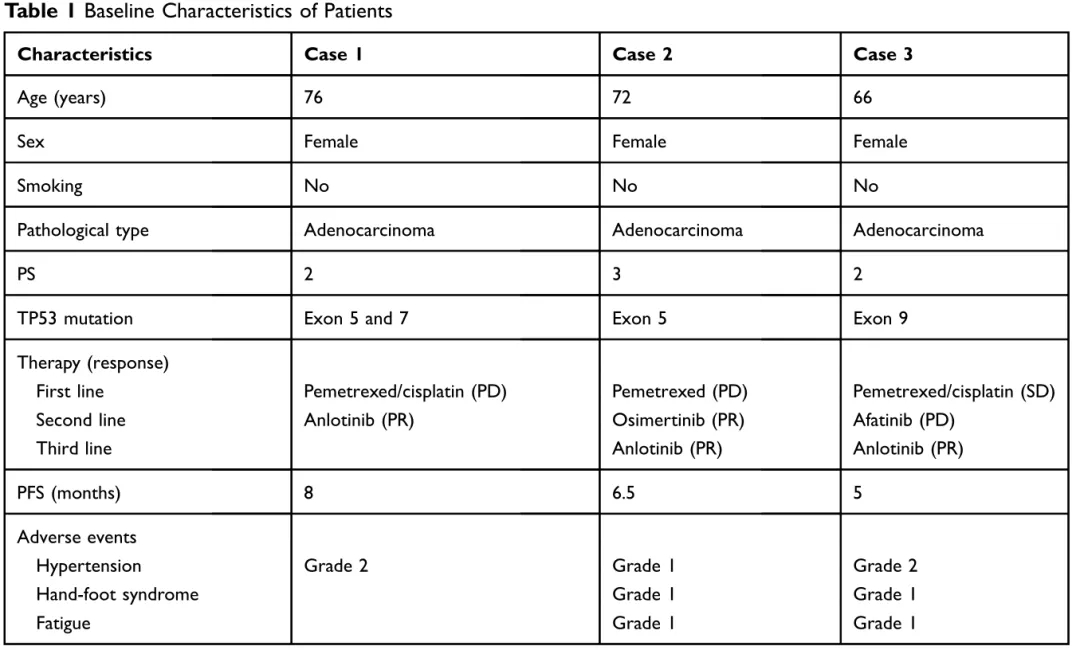
1 案例一
2 案例二
3 案例三
01
拨开迷雾 泛癌种靶点TP53或成为抗血管生成药物的预测因子
02
TP53在多癌种抗血管生产药物治疗中体现很好的预测作用
3.胰腺癌
凡德他尼小分子多靶点酪氨酸激酶抑制剂,靶点包括EGFR、VEGFR 2和RET等,研究显示,伊立替康和凡德他尼治疗TP53和KRAS突变的胰腺癌患者具有很好的临床价[9]。
4.胃癌
雷莫芦单抗是一个血管内皮生长因子受体2(VEGFR2)拮抗剂特异性地与VEGF受体2结合和阻断VEGFR配体,VEGF-A,VEGF-C,和VEGF-D与受体的结合。
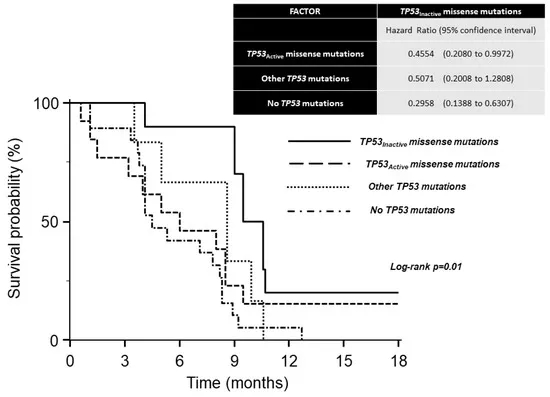
在一项研究雷莫芦单抗联合紫杉醇二线治疗胃癌患者的研究中[10],48位患者中,二线治疗的结果显示ORR为20.8%,中位os为8.4个月。
不同基因状态中位OS时间为:TP53 非活性错义突变携带者9.5个月;其他TP53突变携带者为8.6个月;TP53 主动错义突变携带者6.0个月;无TP53突变的患者4.5个月。
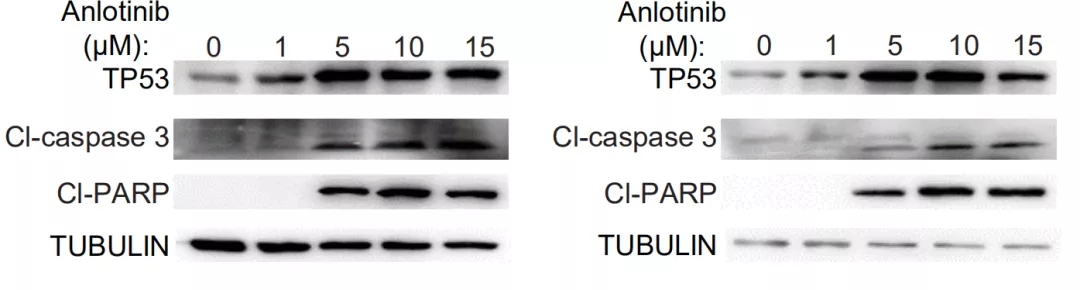
与上述多靶点抗血管生成药物相似,安洛替尼也主要通过抑制VEGFR1-3和成纤维细胞生长因子受体(FGFR)1-4。本文中三个临床案例均具有TP53突变,接受安罗替尼治疗后效果均为PR。基于这些以上数据,TP53突变患者可能是安罗替尼获益人群。当然更需要一个更大的临床前瞻性的随机对照试验来确认!小火苗,大希望!期待这一发现成为我们打开TP53突变肿瘤治疗的契机!
参考文献
[1]Fang S, Cheng W, Zhang M, Yang R. Association of TP53 Mutations with Response to Anlotinib Treatment in Advanced Non-Small Cell Lung Cancer. Onco Targets Ther. 2020;13:6645-6650. Published 2020 Jul 7. doi:10.2147/OTT.S257052
[2] Li AM, Boichard A, Kurzrock R. Mutated TP53 is a marker of increased VEGF expression: analysis of 7525 pan-cancer tissues. Cancer Biol Ther. 2020:1–6.
[3]Wheler JJ, Janku F, Naing A, et al. TP53 alterations correlate with response to VEGF/VEGFR inhibitors: implications for targeted therapeutics. Mol Cancer Ther. 2016;15(10):2475–2485. doi:10.1158/ 1535-7163.MCT-16-0196
[4]Wheler JJ, Janku F, Naing A, et al. TP53 alterations correlate with response to VEGF/VEGFR inhibitors: implications for targeted therapeutics. Mol Cancer Ther. 2016;15(10):2475–2485. doi:10.1158/ 1535-7163.MCT-16-0196
[5]Fu S, Hou MM, Naing A, et al. Phase I study of pazopanib and vorinostat: a therapeutic approach for inhibiting mutant p53-mediated angiogenesis and facilitating mutant p53 degradation. Ann Oncol. 2015;26(5):1012–1018. doi:10.1093/annonc/mdv066
[6]Koehler K, Liebner D, Chen JL. TP53 mutational status is predictive of pazopanib response in advanced sarcomas. Ann Oncol. 2016;27 (3):539–543. doi:10.1093/annonc/mdv598
[7]Wu Y, Huang J, Wang Q, et al. Whole-exome sequencing insights into pulmonary artery sarcoma mimicking pulmonary embolism: a case report and review. Onco Targets Ther. 2019;12:6227–6235. doi:10.2147/OTT.S212416
[8]Ruan X, Shi X, Dong Q, et al. Antitumor effects of anlotinib in thyroid cancer. Endocr Relat Cancer. 2019;26(1):153–164. doi:10.1530/ERC-17-0558
[9]Kaushik AC, Wang YJ, Wang X, Wei DQ. Irinotecan and vandetanib create synergies for treatment of pancreatic cancer patients with concomitant TP53 and KRAS mutations [published online ahead of print, 2020 Jul 31]. Brief Bioinform. 2020;bbaa149. doi:10.1093/bib/bbaa149
[10]Graziano F, Fischer NW, Bagaloni I, et al. TP53 Mutation Analysis in Gastric Cancer and Clinical Outcomes of Patients with Metastatic Disease Treated with Ramucirumab/Paclitaxel or Standard Chemotherapy. Cancers (Basel). 2020;12(8):E2049. Published 2020 Jul 24. doi:10.3390/cancers12082049