科学家发现肿瘤微环境促进肿瘤生长的“秘密”
就像植物生长需要营养丰富的土壤和水源一样,肿瘤周围的组织、免疫细胞、血管和细胞外基质共同形成的“肿瘤微环境”也“帮助”肿瘤更快地进行增殖和“侵略”。缺少土壤和水源,植物就会枯死,那么如果抑制肿瘤微环境,是不是也可以阻止肿瘤的生长呢?
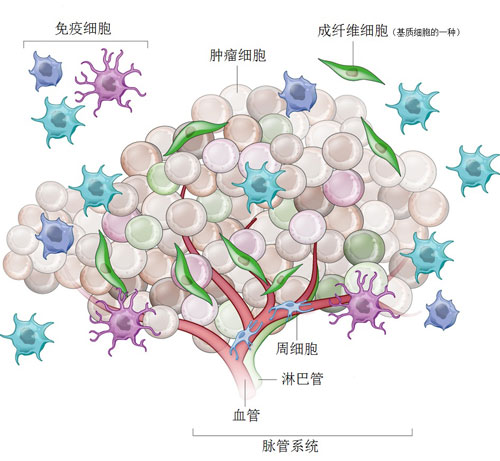
肿瘤微环境
索尔克研究所的研究人员也有此想法,他们通过体外模拟发现了肿瘤是如何与其微环境相互作用,达到快速生长的目的的。不仅如此,他们还发现,抑制微环境中的信号通路,就可以抑制肿瘤的生长。这些研究成果发表在了《美国国家科学院院刊》上 [1]。
研究选用的是胰腺癌模型,胰腺癌的难治程度是“有目共睹”的,五年生存率仅有 5% 左右,当年的乔帮主也是用尽了各种方法,在和胰腺癌抗争了 8 年后仍然没能“赢得这场战争”。研究的通讯作者,索尔克研究所基因表达实验室的主任 Ronald Evans 说,化疗和免疫疗法对胰腺癌都不是十分有效,因此需要研究人员开发新的途径去治疗。

Ronald Evans(左一)和他的研究团队
人体内有一类细胞叫做基质细胞,它们可以构成器官内的结缔组织,起到支持和提供营养的作用。在过去的研究中,科学家们发现,肿瘤微环境中的基质细胞既可以发出支持肿瘤生长的信号,也可以发出抑制肿瘤生长的信号 [2],于是,Evans 教授和他的团队希望能够明确地揭示出癌细胞是如何利用支持性信号来帮助自己生长的。
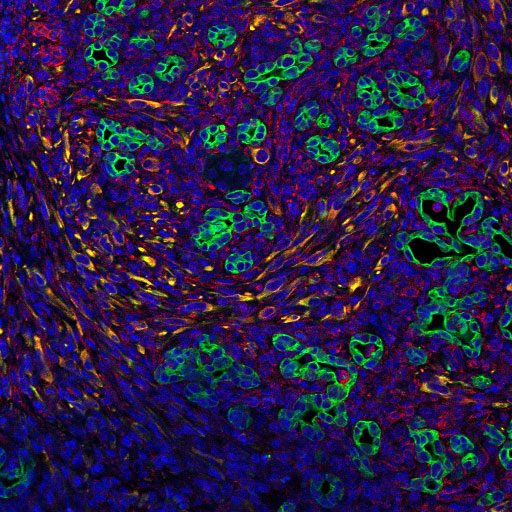
荧光成像图,绿色为癌细胞,红色为基质细胞
为了这个目标,研究人员们构建了一个三维培养体系,他们可以在这其中培养人类的胰腺肿瘤细胞,观察在有基质细胞信号和缺少基质细胞信号的条件下,肿瘤细胞如何生长、发生怎样的变化。经过对比分析,研究人员发现在有基质细胞信号存在的条件下,胰腺肿瘤细胞的代谢速度变快了,而且代谢物的组成水平发生了变化。涉及代谢过程的基因中,基质细胞信号诱导 DNA 上的组蛋白“乙酰化”,有 2 个基因的表达量因此增加。
这是怎么回事呢?首先,在细胞核中,组蛋白能够与 DNA 结合。其次,“组蛋白乙酰化”是一种表观遗传学修饰,乙酰基就好像是一个“标签”被“贴到”了组蛋白上,而这个“标签”决定了 DNA 在转录的时候对对应转录区域进行识别并转录,进而完成基因的表达。所以,当有“额外的”组蛋白乙酰化后,DNA 进行了“额外的”转录,基因的表达量也就增加了。因此,研究人员想到,如果通过抑制剂来抑制这个过程,是不是就可以解决基因表达量增加和代谢变快的问题呢?根据过去的研究,他们选择了一种叫做 JQ1 的抑制剂,它的作用是阻止标签发挥作用,让这些 DNA 不能进行“额外的”转录,它的表达量也就不会因此而增加了 [3]。
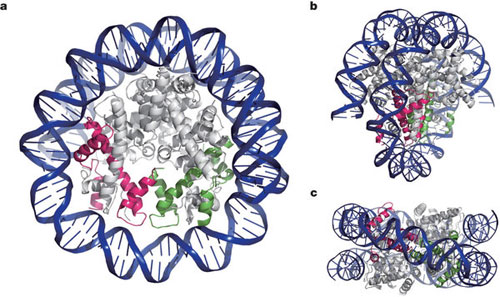
DNA 与组蛋白结合的三视图
果然,当 JQ1 加入培养体系后,即使有基质细胞信号的存在,2 个基因的表达量也没有出现之前一样的升高情况,代谢速度也恢复了正常。为了进一步证实 JQ1 在体内是否也有效果,研究人员在胰腺癌小鼠中也进行了实验。经过 14 天的治疗,小鼠体内胰腺肿瘤的增长显著减慢,在实验结束后,研究人员发现胰腺癌小鼠的胰腺重量比治疗前降低了。接下来,研究人员希望能够更加深入地研究肿瘤微环境中是否还有其他途径能够支持肿瘤的生长,以及怎样的剂量范围既能够抑制甚至减小肿瘤还能够保证安全性。总之,这个研究为科学家在攻克肿瘤的道路上,又提供了一种新的可能性。
参考文献:
[1] Sherman M H, Ruth T Y, Tseng T W, et al. Stromal cues regulate the pancreatic cancer epigenome and metabolome[J]. Proceedings of the National Academy of Sciences, 2017: 201620164.
[2] Rhim AD, et al. (2014) Stromal elements act to restrain, rather than support, pancreatic ductal adenocarcinoma. Cancer Cell 25(6):735–747
[3] Jostes S, Nettersheim D, Fellermeyer M, et al. The bromodomain inhibitor JQ1 triggers growth arrest and apoptosis in testicular germ cell tumours in vitro and in vivo[J]. Journal of Cellular and Molecular Medicine, 2016.