在研新药一线治疗肝细胞癌 3 期达所有终点
6 月 5 日,Eisai 公司公布了 3 期 REFLECT 研究(研究 304)的结果,使用多重受体酪氨酸激酶抑制剂 Lenvima( lenvatinib )一线治疗手术不可切除的肝细胞癌(uHCC)患者。在临床试验中,lenvatinib 表现出整体生存(OS)的非劣效性,达到了该研究的主要终点;与 sorafenib 相比,lenvatinib 还达到了无进展生存期(PFS)、进展时间(TTP)和客观缓解率(ORR)的次要终点,具备统计学显著性和临床意义的改善。这些数据在芝加哥举行的美国临床肿瘤学会(ASCO)2017 年年会上(摘要 4001)以口头汇报形式公布。
肝细胞癌是最常见的肝癌,约占美国原发性肝癌的 90%。2015 年,全球肝癌死亡人数约为 78.8 万,是全球癌症相关死亡的第二大原因。过去十年来,肝癌的发病率和死亡率稳步上升。今年,美国将新增确诊 4 万多例肝癌,近 3 万人将死于该疾病。uHCC 一般处于疾病的 3 级或 4 级阶段,是肝癌的晚期阶段,不能通过手术去除。大约 45%的患者在确诊时已经是 3 级或 4 级肝细胞癌。针对这些晚期疾病患者,治疗方案非常有限。

由 Eisai 发现和开发的 lenvatinib 是抑制血管内皮生长因子(VEGF)受体 VEGFR1- 3 激酶活性的受体酪氨酸激酶(RTK)抑制剂。Lenvatinib 还可有效抑制与病原性血管发生、肿瘤生长和癌症进展相关的其他 RTK,包括成纤维细胞生长因子(FGF)受体 FGFR1-4、血小板衍生生长因子受体α(PDGFRα)、KIT 和 RET。
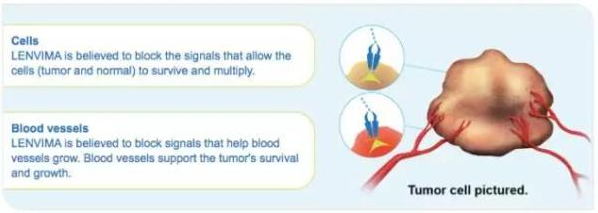
▲Lenvima 的作用机理(图片来源:Lenvima 官网)
作为一种激酶抑制剂,Lenvima(lenvatinib)获批适用于:
分化甲状腺癌(DTC):针对局部复发或转移、进行性、放射碘剂难治性 DTC 患者的单一药物。
肾细胞癌(RCC):先前的抗血管生成治疗方案之后,结合 everolimus 治疗晚期肾细胞癌(RCC)患者。
REFLECT 是一项国际多中心、随机、开放标签、非劣效的 3 期研究,用于比较 lenvatinib 与 sorafenib 作为 uHCC 患者一线治疗的疗效和安全性。954 名患者被随机分入 21 个国家的 183 个试验点,每天接受 12 毫克或 8 毫克 lenvatinib(n=478),或每日两次 400 毫克 sorafenib(n=476),治疗持续到疾病进展或不可接受的毒性。这项研究的主要终点是总体生存(OS)。本研究的次要疗效终点是无进展生存期(PFS)、进展时间(TTP)和客观反应率(ORR)。
接受 lenvatinib 治疗患者的中位 OS 为 13.6 个月,sorafenib 为 12.3 个月(HR:0.92; 95%CI:0.79±1.06)。接受 lenvatinib 治疗组患者的中位 PFS 为 7.4 个月,中位 TTP 为 8.9 个月,sorafenib 组中位 PFS 为 3.7 个月(HR:0.66; 95%CI:0.57 0.77; p<0.00001),中位 TTP 为 3.7 个月(HR 0.63; 95 %CI; 0.53 0.73; p<0.00001)。此外,与 sorafenib 相比,lenvatinib 显示出显着更高的 ORR(24%)(优势比:3.13; 95%CI:2.15-4.56; p<0.00001)。

“作为一家不懈努力,服务于难治癌症患者的公司,Eisai 对研究 304 中 lenvatinib 展示潜力感到兴奋:它为需要额外治疗方案的不可切除 HCC 患者提供了改善的疗效结果,”Eisai 肿瘤部门的首席临床官兼首席医学官 Alton Kremer 博士说道:“根据这些数据,Eisai 计划提交针对 lenvatinib 的监管申请,以便对不可切除的 HCC 患者进行潜在的一线疗法。我们期待与 FDA 以及全球范围内的其他监管机构紧密合作。”
参考资料:
[1] Eisai Inc. (ESALF.PK) Release: Lenvatinib Demonstrates Positive Results Vs Sorafenib Across All Endpoints In First-Line Phase III Non-Inferiority Trial Of Unresectable Hepatocellular Carcinoma (uHCC)
[2] Eisai Inc. 官方网站