Pemigatinib 佩米替尼/培米替尼 (Pemazyre,达伯坦)治疗胆管癌的临床研究数据如何?
培米加替尼用于治疗已经扩散或无法通过手术切除的胆管癌(胆管癌),用于之前已经尝试过癌症治疗且癌症中具有某种类型的异常FGFR2基因的患者。您的医生将测试该基因的存在。
培米替尼还用于治疗癌症中具有某种异常FGFR1基因的患者复发或对治疗无反应的骨髓/淋巴样肿瘤(血癌)。您的医生将测试该基因的存在。
培米替尼是一种抗肿瘤(癌症)药物。它干扰癌细胞的生长,最终被身体破坏。
培米加替尼只能通过医生的处方获得。那么培米替尼(pemigatinib)在治疗胆管癌的临床研究数据如何?
FIGHT-202 (NCT02924376) 是一项多中心开放标签单臂试验,评估了 PEMAZYRE 在 107 例局部晚期不可切除或转移性胆管癌患者中的疗效,这些患者的疾病在至少 1 次先前治疗中或之后进展,并且通过中心实验室进行的临床试验测定确定 FGFR2 基因融合或非融合重排。预计合格的帧内融合和其他重排在FGFR17基因的内含子18/外显子2内有一个断点,使FGFR2激酶结构域完好无损。
患者以21天为周期接受PEMAZYRE,剂量为13.5mg口服,每日一次,连续14天,然后停止治疗7天。给予PEMAZYRE直到疾病进展或不可接受的毒性。主要疗效结局指标是总体缓解率(ORR)和缓解持续时间(DoR),由独立审查委员会(IRC)根据RECIST v1.1确定。
中位年龄为56岁(范围:26至77岁),61%为女性,74%为白人,95%的基线东部肿瘤合作组(ECOG)表现状态为0(42%)或1(53%)。2%的患者患有肝内胆管癌。2%的患者进行了框内FGFR2基因融合,最常见的FGFR1融合是FGFR34-BICC2(1%)。27%的患者有其他FGFR2重排,不能自信地预测为帧内融合,包括没有可识别伴侣基因的重排。所有患者既往至少接受过 12 线全身治疗,3% 既往接受过 76 线治疗,<>% 患者既往接受过 <> 线或更多治疗。<>%的患者既往接受过铂类药物治疗,其中<>%的患者既往接受过吉西他滨/顺铂治疗。
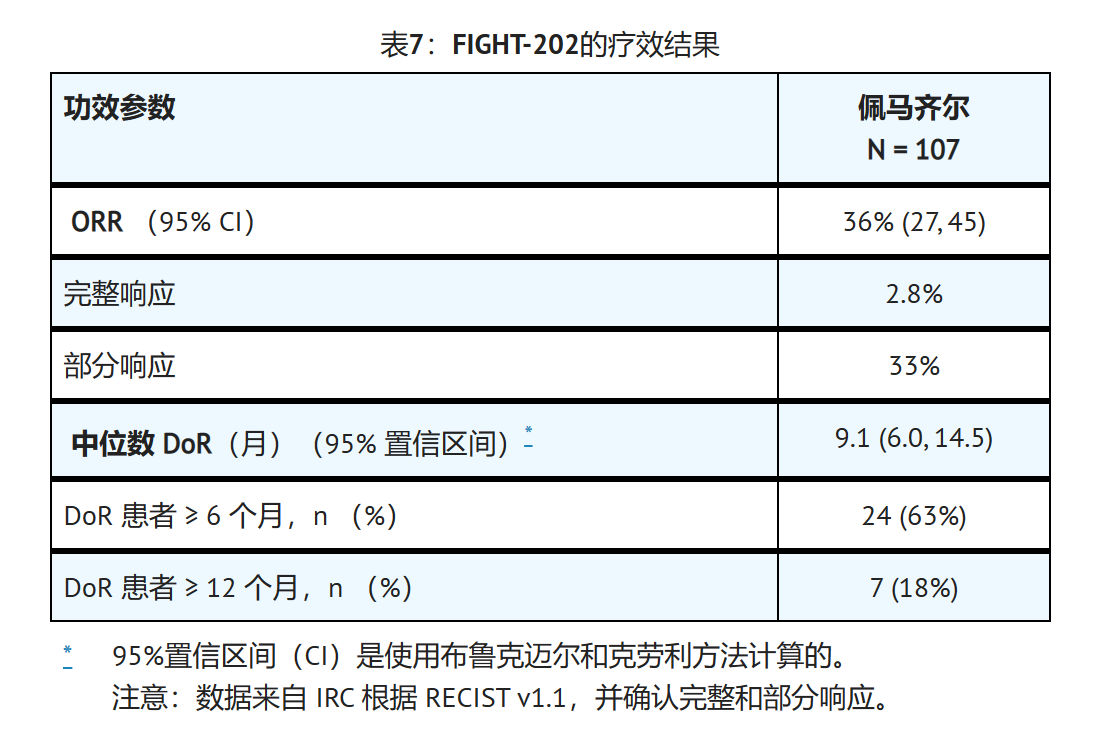
疗效结果总结于表7。
中位缓解时间为2.7个月(范围0.7-6.9个月)。